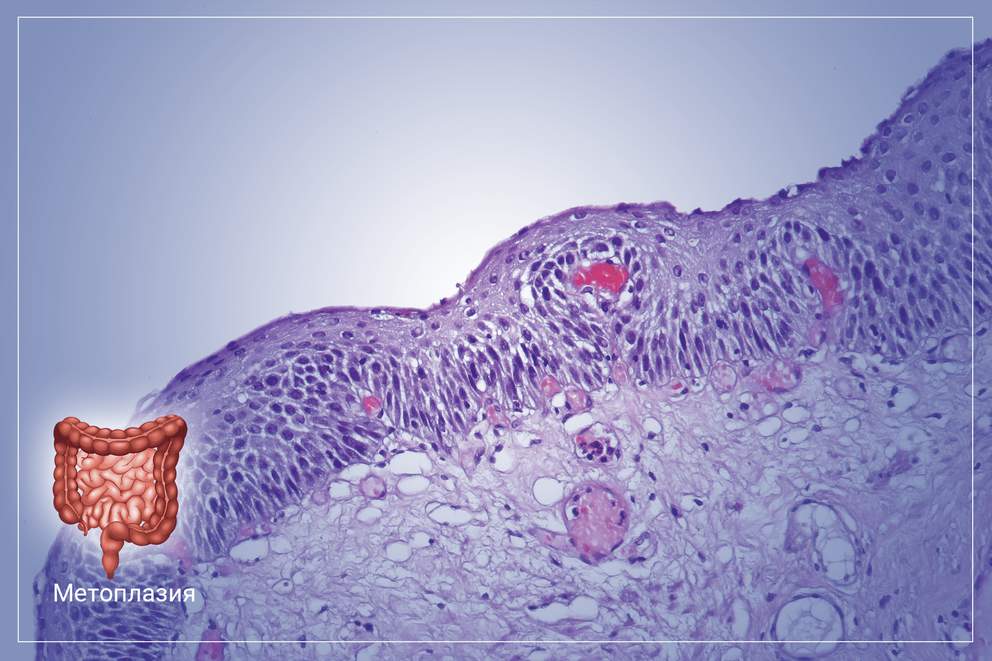
Пролиферация клеток железистого эпителия желудка что это
Как облегчить состояние при кишечной метаплазии
Хроническое воспаление слизистой оболочки желудка на фоне нерационального питания, злоупотребления алкоголем и приема отдельных групп лекарственных медикаментов, со временем может привести к развитию кишечной метаплазии. Чаще всего заболевание диагностируется у людей средней возрастной группы и пожилых пациентов. Эта патология сопровождается характерными клиническими симптомами и негативно отражается на общем состоянии человека.
Что такое метаплазия
В основе этого заболевания лежит планомерная атрофия эпителия слизистой оболочки желудка, с последующим его замещением на эпителий толстого или тонкого кишечника. Изменённая слизистая оболочка начинает выполнять функции того органа, к которому оно принадлежит по факту. Таким образом, желудок теряет свои функции как орган пищеварения со всеми вытекающими последствиями. Метаплазия относится к редким патологиям пищеварительной системы, при этом не является самостоятельным заболеванием, а возникает только при длительном хроническом повреждении слизистой оболочки органа на фоне воспалительного процесса. Это заболевание несет прямую угрозу не только здоровью, но и жизни человека. Несмотря на это, своевременная диагностика и комплексное лечение дают все шансы на полное выздоровление.
Виды метаплазии
В гастроэнтерологии выделяют такие разновидности кишечной метаплазии или атрофии:
Кроме перечисленных двух видов, может развиваться и смешанный вариант кишечной метаплазии слизистой, при котором в желудке обнаруживаются клетки эпителия как толстого, так и тонкого кишечника.
По степени распространённости выделяют такие формы метаплазии:
Существует также классификация данного заболевания по характеру распространения. Выделяют такие разновидности метаплазии:
Абсолютная тонкокишечная метаплазия
Эта форма метаплазии характеризуется появлением клеток эпителия тонкого кишечника по всей площади желудка. Характерным признаком абсолютной тонкокишечной метаплазии является появление клеток Панета. По структуре и функциональным особенностям, желудок полностью напоминает тонкий кишечник. Эта форма метаплазии чаще сопровождается хроническим гастритом.
Частичная толстокишечная метаплазия
Для этой формы заболевания не характерно появление клеток Панета, но при этом наблюдается появление эпителиальных клеток, которые выстилают внутреннюю поверхность толстого кишечника. При толстокишечной метаплазии может нарушаться процесс дифференцирования и созревания клеток, что указывает на высокую вероятность образования злокачественной опухоли.
Причины возникновения
Первопричины развития данного состояния до конца не установлены, но существует ряд предрасполагающих факторов, которые могут спровоцировать развитие метаплазии. К таким факторам можно отнести:
Клинические симптомы
Для каждой формы метаплазии характерны свои симптомы, но существует ряд признаков, которые указывают на развитие данного состояния. К таким признакам относят:
Диагностика
Наиболее информативным методом диагностики метаплазии является фиброгастродуоденоскопия, с помощью которой удается не только обнаружить патологически измененные очаги на стенках желудка, но и взять образец биоматериала для последующего гистологического анализа. В отдельных случаях применяется методика гастроскопии с использованием контраста (хромогастроскопия). В качестве окрашивающего вещества используется метиленовый синий.
Лечение
Комплексное лечение включает использование безоперационных и хирургических методов. Лечение назначается индивидуально, при этом во внимание берутся такие факторы, как возраст пациента, результаты обследования и наличие сопутствующих заболеваний. Медикаментозное лечение может включать прием таких групп лекарственных медикаментов:
При кишечной метаплазии желудка очень важно позаботиться о нормализации микрофлоры, так как при нарушении баланса микроорганизмов в желудке и кишечнике страдает не только иммунитет, но и подрывается здоровье всего ЖКТ. Свою эффективность в восстановлении кишечной и желудочной микрофлоры доказал метапребиотик Стимбифид Плюс, содержащий натуральную питательную среду для полезных микроорганизмов, обитающих в просвете ЖКТ. Стимбифид Плюс не только восстанавливает нормальный баланс бактерий при хроническом гастрите, но и ускоряет процесс восстановления эпителия желудка, препятствуя дальнейшему прогрессированию метаплазии.
Процессы регенерации в слизистой оболочке желудка и канцерогенез
В клинической практике гастроэнтерологов нередко возникает необходимость воздействовать на процессы регенерации в гастродуоденальной зоне. В последние годы в связи с успехами молекулярной биологии существенно изменились представления о механизмах регуляции репаративных процессов. Воздействие на эти процессы требует осторожного подхода и глубокого понимания основных закономерностей.
Следует осознать, что вычленение отдельных компонентов этих процессов и воздействий регуляторных факторов носит условный характер, так как в организме они тесно связаны и переплетены между собой. После ознакомления с современными взглядами на общие закономерности регенераторных процессов мы конкретизируем их в отношении слизистой оболочки желудка, в частности в условиях геликобактерной инфекции.
Регенерацией (возрождением) называют процесс восстановления разрушенных или утраченных тканей, органов и отдельных частей тела живых существ.
Различают физиологическую и репаративную регенерацию.
В многоклеточном организме физиологической регенерацией называют процесс постоянного обновления клеток различных тканей. Биологический смысл процесса регенерации у многоклеточного организма заключается в восстановлении структуры, способной к выполнению специализированной функции. Достигается это либо восстановлением клеточной массы органа за счет гиперплазии клеток (клеточный тип регенерации), либо путем гиперплазии клеточных ультраструктур (внутриклеточный тип регенерации).
В ходе репаративной регенерации при восстановлении клеток, поврежденных патологическим процессом, включаются дополнительные механизмы, способствующие ускорению клеточного обновления. Репаративная регенерация может быть полной (реституция) при замещении дефекта тканью идентичной предсуществовавшей ткани и неполной (субституция), когда дефект ткани замещается тканью с более низким уровнем организации, например рубцом. В последние годы установлено, что при репаративной регенерации в органах формируются принципиально новые клеточные линии с новыми функциональными свойствами.
Основными компонентами регенераторного процесса являются: клеточная пролиферация и дифференцировка, миграция клеток, а также реструктуризация стромы и ангиогенез.
Реструктуризация стромы заключается в изменении клеточного состава и компонентов межклеточного матрикса собственной пластинки слизистой оболочки.
Процессы пролиферации и дифференцировки клеток в нормальных тканях организма теснейшим образом связываются понятием «клеточный путь».
Процессы пролиферации и дифференцировки клеток в ходе клеточного цикла идут параллельно и относительно автономно. Судьба клетки зависит от того, какой из этих процессов протекает быстрее.
Если подготовка к митозу произойдет быстрее, то клетка переходит в G1 фазу, и ее деление будет неизбежным. В противном случае клетка успеет продвинуться по пути дифференцировки настолько, что перейдет в фазу G0 следующего цикла (G0′). Длительность последней больше, чем фаза G0 предыдущего цикла, но теперь и времени для формирования механизмов митоза требуется больше. Время генерации клетки приближается ко времени ее жизни. Вероятность вступления в митоз уменьшается.
Английский эмбриолог Уодингтон предложил для описания представления о дифференцировке модель наклонной плоскости, по которой катится шарик. Недетерминированная клетка проходит при этом определенные дифференцировочные уровни, порог которых при нормальных условиях преодолим лишь в одном направлении.
На определенных этапах пути шарик попадает в дифференцировочные ямы, отражающие состояние относительной стабильности. Выйти из этого состояния клетка может в трех направлениях:
Схематически низший уровень на такой плоскости соответствует максимальной дифференцировке, то есть клетке с легко верифицируемым фенотипом, а схематически высший уровень соответствует идеальной зародышевой клетке, из которой может быть получен любой клеточный тип, входящий в организм данного вида.
В генетическом отношении дифференцировка клеток не является следствием коренных изменений генома, а определяется физико-химическими факторами, влияющими на геном. Разобщенные клетки не способны к дифференцировке. Дифференцировка одной клетки или клеток, изолированных друг от друга, невозможна.
Эксперименты с пересадкой ядер показали, что дифференцировка не связана с утратой или добавлением генетической информации. Ядро клетки любой ткани организма содержит одну и ту же генетическую информацию, но в большинстве дифференцированных клеток эта информация надежно заблокирована.
По теории открытого генома генетическая информация в недифференцированной клетке полностью открыта. Открытыми называются участки ДНК, доступные для молекул РНК-полимеразы, и, следовательно, для транскрипции с последующим синтезом белка.
Допускается, что в идеальной зародышевой клетке могут синтезироваться (хотя и в минимальных количествах) все белки, возможные для данного организма.
По мере дифференцировки происходит открытие одних генов и закрытие других. На разных стадиях развития и у клеток различных типов различны и зоны открытой ДНК. Закрытие генов осуществляется путем связывания нитей ДНК с основными белками гистонового типа. При этом блокированные участки ДНК приобретают компактную конфигурацию и становятся недоступными для транскрипции.
Исходя из положений этой теории легко понять молекулярную суть процесса детерминации, которая заключается в предварительном синтезе информационной РНК и накоплении ее в цитоплазме частично детерминированной клетки. Специфических белков в клетке еще нет, фенотип клетки еще не проявился, но иРНК для его синтеза уже готова. При получении очередных регуляторных стимулов синтез белка начинается, и клетка приобретет соответствующий фенотип.
По мере дальнейшей дифференцировки весь синтетический потенциал клетки переключается на продукцию специфических белков, что приводит к формированию фенотипа клетки, дифференцированной в определенном направлении. Подтверждением такому ходу событий является обнаружение в различных органах клеток-микстов, то есть клеток, сочетающих в себе фенотипические признаки нескольких видов клеток.
В желудке методами гибридизации in situ были выявлены клетки, экспрессирующие мРНК одновременно к гастрину и соматостатину, то есть эта частично детерминированная клетка «определилась» с направлением дифференцировки в сторону эндокринных клеток, но «не решила» стать гастриновой G-клеткой или соматостатиновой D-клеткой.
Таким образом, именно процесс поэтапного блокирования одних генов и разблокирования других является основой механизмов дифференцировки. Осуществляется этот процесс путем индукции, то есть влияния внешних факторов и клеток друг на друга.
Регенерация тканей взрослого организма представляет собой каскад индукций. В результате сбоя этих регулировочных механизмов возможно формирование клеточных линий, утрачивающих способность к дифференцировке или с преобладанием пролиферативного компонента. Это одно из основных патогенетических звеньев канцерогенеза.
Начало изучению гуморальных механизмов клеточного обновления в желудке было положено открытием трофического действия гастрина и «антитрофического» действия соматостатина.
Действие соматостатина на слизистую оболочку желудка можно назвать «антитрофическим» лишь условно, так как непосредственного влияния на пролиферативные процессы этот гормон не оказывает. Однако он обладает свойством подавлять секрецию гастрина, а также разнообразных биологически активных веществ, усиливающих пролиферативные процессы.
Блокирование пролиферативных и моторных стимулов соматостатином приводит к удлинению фазы покоя (G0) клеточного цикла и тем самым создает благоприятные условия для процессов клеточной дифференцировки. Секретируется соматостатин D-клетками антрального отдела желудка. В меньшем количестве и более равномерно D-клетки распределены и по другим отделам желудочно-кишечного тракта.
Факторы роста представляют собой самую многочисленную группу индукторов пролиферации и дифференцировки клеток. Эпидермальный фактор роста (EGF), который продуцируется клетками слюнных желез и выделяется со слюной, а также трансформирующий фактор роста a (TGF-a) и инсулиноподобный фактор роста (IGF) усиливают клеточную пролиферацию и угнетают процессы дифференцировки.
Трансформирующий фактор роста b (TGF-b) обладает прямо противоположным действием. Он ингибирует клеточную пролиферацию и способствует дифференцировке клеток.
Фактор роста кератиноцитов (KGF) стимулирует как пролиферацию, так и дифференцировку клеток.
TGF-a цитохимически выявляется на мембранах тубуловезикул париетальных клеток и в цитомембранах главных клеток. Он способствует подавлению кислой желудочной секреции и является сильным митогеном, то есть способствует заживлению язвенного дефекта.
EGF и TGF-a обладают вазодилатирующими свойствами, способствуя ангиогенезу в области язвенного дефекта и усиливая репаративные процессы. Однако увеличение экспрессии рецепторов к EGF, что наблюдается во всех случаях рака желудка независимо от гистологического типа, повышает восприимчивость опухолевых клеток к стимулам, усиливающим пролиферацию.
К недавно открытым регуляторам клеточного цикла относится и семейство трефоиловых пептидов, получившие название по своеобразной трехлопастной структуре своих молекул.
Пространственная структура трефоиловых пептидов представляет собой три петли, состоящие из полипептидных цепей, соединенных дисульфидными мостиками. Они продуцируются слизеобразующими клетками слизистой оболочки желудка и кишки в норме, но их продукция многократно возрастает при образовании дефекта эпителиального пласта.
По данным электронно-микроскопической иммуноцитохимии, Ps2 и hSp локализуются на цитомембранах, включая мембраны комплекса Гольджи слизеобразующих клеток. Они включаются в состав слизистых гранул, вместе с которыми и высвобождаются в просвет.
Все трефоиловые пептиды существенно замедляют рост опухолевых клеток. Эти вещества чрезвычайно устойчивы к действию пищеварительных ферментов и оказывают регуляторные воздействия, находясь в просвете желудочно-кишечного тракта. Интересно, что они присутствуют и в цитомембранах эндокринных клеток желудочно-кишечного тракта, включаются в состав их эндокринных гранул, вместе с которыми секретируются в собственную пластинку слизистой оболочки. Значение этого регуляторного механизма пока не изучено.
Комбинированное воздействие факторов роста и трефоиловых пептидов позволяет оптимизировать процессы регенерации за счет уменьшения пролиферативного компонента.
Для реализации своих функций р53 нуждается в генах семейства bcl, белковые продукты которых оказывают порой диаметрально противоположное действие на апоптоз и пролиферацию. Так, белок bcl-2 подавляет апоптоз через блокаду кальциевых каналов клеточных мембран, усиливает пролиферацию и способствует дифференцировке клеток.
Местом локализации bcl-2 в клетке являются внутренние мембраны митохондрий и ядро клетки. Другие гены этого семейства (Bax, bclXS), наоборот, синнергически взаимодействуют с р53, подавляя пролиферацию и усиливая апоптоз.
Таким образом, баланс между белковыми продуктами этих генов определяет равновесие между пролиферацией и апоптозом.
Такие составные компоненты межклеточного вещества, как Е-кадгерин и коллаген IV, подавляют миграцию клеток вне генеративных зон, создавая условия для их дифференцировки, не воздействуя на процессы пролиферации. Е-кадгерин используется для построения плотных межклеточных контактов. Роль его в норме мало изучена. Он препятствует обратной диффузии кислот (но не щелочей) из просвета желудка.
Мутациям генов, кодирующих синтез молекул адгезии, придается большое значение в механизмах инфильтративного роста и метастазирования опухолей. За последние 3 года резко возросло количество публикаций, посвященных этому вопросу. Основной их смысл сводится к тому, что рост опухоли (как пролиферация) и инвазия регулируются различными механизмами. При этом главным в механизмах инвазивного роста является снижение экспрессии или мутация генов адгезивных молекул, в частности Е-кадгерина.
Мутации в генах, кодирующих синтез Е-кадгерина, приводят к развитию диффузного рака желудка с ранним метастазированием и плохим прогнозом. Заболевание это имеет семейный характер. Такие мутации не встречаются при раке желудка кишечного типа. Тест на выявление растворимых фрагментов Е-кадгерина в крови рекомендуется для использования в качестве маркера диффузного рака желудка.
Линии эндокринных, главных и париетальных клеток в области шеечных отделов желез проходят стадию клеток-предшественников. Процессы дифференцировки различных клеточных линий могут регулироваться автономно под влиянием различных гуморальных факторов клеточного микроокружения.
Согласно данным, полученным в последнее время на трансгенных мышах, париетальные клетки играют решающую роль в механизмах дифференцировки шеечных клеток в главные клетки. Репаративная регенерация при острых повреждениях слизистой оболочки желудка осуществляется по типу реституции с полным восстановлением структуры и функции.
Однако при хронических патологических процессах часто возникают сбои в работе регуляторных механизмов клеточной пролиферации и дифференцировки, что приводит к субституции (атрофия главных желез при атрофическом гастрите, образование рубца на месте хронической язвы) либо к патологической регенерации (кишечная метаплазия). После гастрэктомии или частичной резекции у взрослого организма полного восстановления желудка как анатомо-физиологического образования не происходит.
Однако исследованиями Н. Райта с использованием современных морфологичесаких, иммуногистохимических методик и методов гибридизации in situ установлено, что эта группа клеток представляет собой отдельную дифференцировочную ветвь, происходящую из стволовых клеток. Эти клетки характеризуются определенным фенотипом: они продуцируют нейтральные мукополисахариды, выявляемые ШИК-реакцией (в отличие от окружающих слизистых клеток, продуцирующих кислые муцины).
Кроме того, они секретируют большое количество регуляторных пептидов и других индукторов пролиферации или дифференцировки окружающих клеток: EGF, TGF-a, FGF, некоторые из трефоиловых пептидов и лизоцим, обладающий бактерицидным действием.
Большой объем информации накоплен по влиянию Helicobacter pylori на процессы пролиферации и дифференцировки клеток в слизистой оболочке желудка. Развитие этой инфекции приводит к усилению пролиферативных процессов в слизистой оболочке желудка. Однако установлено, что эффект этот обусловлен не прямым действием H. pylori, а опосредован повышением уровня гастрина в крови.
Следствием прямого непосредственного действия H. pylori на эпителиальные клетки желудка является усиление апоптоза. Действие это проявляется как при геликобактерном гастрите, когда задействованы все механизмы воспалительных реакций, так и in vitro на культуре эпителиальных клеток желудка, когда участие факторов воспалительной реакции исключается. При этом не только усиливается апоптоз, но и наблюдается фрагментация ДНК.
Известно также, что в условиях геликобактерной инфекции уровень образования активных форм кислорода в слизистой оболочке желудка всегда выше, чем в отсутствие H. pylori, даже при одинаковой степени инфильтрированности ее нейтрофилами и макрофагами. Исходя из этих данных следует подчеркнуть, что весьма важным фактором профилактики рака желудка являются антиоксидантные ферменты и витамины (Е), существенно снижающие риск развития этого заболевания.
Эпителий слизистой желудка с умеренной пролиферацией
Предраковые заболевания желудка
Облигатный предрак — заболевания, на почве которых всегда или в большинстве случаев, если их не лечить, возникает рак. К таким заболеваниям относят каллезную язву желудка, ригидный антральный гастрит, полипы, полипоз желудка.
факультативный предрак — хронические заболевания желудка, при которых рак развивается относительно редко, но чаще, чем У здоровых людей. Это хронический атрофический гастрит, болезнь оперированного желудка, пернициозная анемия, болезнь Менетрие и др.
Национальный раковый конгресс в Японии трактует ряд заболеваний, на фоне которых может возникнуть рак желудка, как фоновые, объединяя в одну группу облигатный и факультативный предрак.
По данным Национального ракового конгресса, рак желудка может развиться на фоне хронического атрофического гастрита в 0-13% случаев, пернициозной анемии — в 0,5-12,3%, хронической язвы желудка — в 1-2%, гиперпластического полипа — в 1-2%, плоской аденомы — в 6-21%, папилловирусной аденомы — в 20-75%, болезни Менетрие — в 5-10%, резекции желудка в анамнезе — в 0,4-7,8% случаев.
С морфологической точки зрения мультицентрически расположенные участки пролиферации атипического эпителия называются дисплазией.
Дисплазия — это нарушение структуры ткани, характеризующееся патологической пролиферацией и атипией эпителия. В слизистой оболочке желудка дисплазия может быть трех степеней (легкая, умеренная и тяжелая).
При дисплазии I и II степени изменения слабо выражены и носят обратимый характер. Изменения же, относящиеся к дисплазии III степени, постоянны и могут рассматриваться как рак in situ. У 40-45% людей в возрасте старше 60 лет в слизистой оболочке желудка происходит перестройка эпителия по кишечному типу — кишечная метаплазия (тонкокишечная, толстокишечная). Толстокишечная метаплазия трактуется как предраковое состояние.
Хронический гастрит — самое распространенное заболевание среди патологии желудочно-кишечного тракта, которое составляет 35% всех болезней органов пищеварения и 85% болезней желудка.
Хронический гастрит — заболевание полиэтиологическое. Существует много причин, вызывающих его, однако в соответствии с этиопатогенезом их можно объединить в три основные группы:
•I группа — инфекционные (экзогенные), связанные с желудочным хеликобактером (гастрит В — бактериальный);
•II группа — эндогенные аутоиммунные, обусловленные образованием антител к обкладочным клеткам желез желудка (гастрит А — аутоиммунный) — атрофический гастрит;
•III группа — экзоэндогенные, связанные с частичными термическими раздражениями, медикаментозными воздействиями выражаются гастродуоденальным рефлюксом (гастрит С — реактивный или химический).
На фоне хронического атрофического гастрита в 0-13% случаев возникает рак желудка.
Клиника. В клинической картине хронического гастрита нет типичных характерных признаков, на основании которых можно было бы распознать те или иные его формы.
Основные жалобы: нарушение аппетита, неприятные ощущения в эпигастральной области, связанные с приемом пищи отрыжка, изжога, тошнота, иногда рвота.
Синдромы желудочной и кишечной диспепсии могут быть в самых различных сочетаниях (чувство переполнения желудка пищей, метеоризм, урчание в животе, тенезмы, запоры, сменяющиеся поносами).
Диагностика. Рентгенологический метод исследования в диагностике хронического гастрита играет относительную роль. Он больше пригоден для выявления язвенного, полипозного и опухолевого поражения желудка. Исключение составляет ригидный антральный гастрит. Решающее значение в распознавании различных форм хронического гастрита принадлежит гастрофиброскопии и гастробиопсии. Диагноз: кишечная метаплазия, дисплазия разной степени выраженности, инфекция, вызванная Helicobacter pylori (HP), — только цитологический и гистологический.
Лечение. К терапевтическим мероприятиям при хроническом гастрите неинфекционной этиологии относятся: устранение основных факторов, способствующих развитию заболевания или поддерживающих его, диетотерапия, седативные средства в период обострений, средства, улучшающие микроциркуляцию и трофику слизистой оболочки, витаминотерапия, санаторно-курортное лечение.
Особого отношения требует инфекционный гастрит, вызванный микроорганизмами Helicobacter pylori. На сегодняшний день учеными мира доказано, что 30-50% населения земного шара — носители HP-инфекции (больной человек или бактерионоситель). HP-бактерии обычно размножаются под слоем слизи над слизистой оболочкой привратника, прикрепляются к апикальной части клеток эпителия, выделяют энзимы — цитотоксины и уреазу, и в эпителии развиваются отек, гиперемия, нарушение трофики, дегенерация клеток слизистой оболочки. Процессы воспаления и атрофии тесно связаны между собой и имеют инфекционно-иммунное происхождение.
В последние 10 лет многих исследователей интересуют проблемы хеликобактериоза и рака желудка. На сегодняшний день доказано, что Helicobacter pylori выpaбатывается множество патогенных ферментов и токсинов, некоторые из них могут быть вовлечены в канцерогенез.
•Показана взаимосвязь между наличием HP-инфекции и кишечной метаплазией, разновидность которой — неполная кишечная метаплазия — считается предраковым состоянием.
•Установлено, что HP с помощью энзима экстрацеллюлярной уреазы расщепляет мочевину с образованием аммиака, активизирует процессы перекисного окисления липидов, повышает концентрацию свободных радикалов — производных кислорода, что стимулирует процессы канцерогенеза.
•В экспериментах in vitro показана способность HP стимулировать рост культуры опухолевых клеток.
Рак желудка в большинстве случаев сопровождается инфицированием слизистой оболочки HP; при этом НР-инфекция имеет большую распространенность, чем при язвенной болезни, приобретает характер тотального обсеменения всех отделов желудка, в том числе и самой опухоли.
Хеликобактерный гастрит (гастрит В) требует особого лечения. Чтобы уничтожить эти бактерии, необходимо обязательное применение трех препаратов, обладающих антибактериальной активностью: амоксициллина или ампициллина, производного нитронидазола (метронидазола) и производного нитрофурина (фуразолидона). Базисный препарат — де-нол (соль лимонной кислоты с висмутом).
Язва желудка. Малигнизация рецидивирующих и каллезных язв желудка отмечается у 2-10% больных.
Клиника. В отличие от хронического гастрита хроническая язва желудка имеет довольно четкую клиническую картину.
Наиболее постоянный симптом язвенной болезни — боль, связанная с приемом пищи. Боли могут быть ранними, возникающими либо сразу после приема пищи, либо через 0,5-1 ч, и поздними, наступающими через 2-3 ч после приема пищи и позднее. Иногда боли возникают ночью и проходят после приема пищи (молока).
Для язвенной болезни желудка характерна также сезонность — обострения в осенне-зимние и весенние месяцы, ремиссии в летний период.
Важным симптомом заболевания является изжога; у большей половины больных бывает рвота, тошнота. В рвотных массах — кислая жидкость с примесью пищи. При рубцовых стенозах привратника рвота становится более частой, при этом рвотные массы обильны, с остатками пищи, съеденной накануне. Нередко отмечаются нарушения функции кишечника — запоры часто сменяются поносами.
Диагностика. В распознавании язвенной болезни желудка, кроме клинической семиотики, определенную роль играет исследование желудочного сока. У большинства больных имеет место повышение секреции и кислотообразования. Лишь при длительном течении заболевания, особенно при каллезных язвах, кислотность желудочного сока понижается. Важно также исследование кала на скрытую кровь.
При рентгенологическом исследовании желудка главным симптомом является ниша. Большая ниша с окружающим валом и конвергенцией складок слизистой оболочки указывает обычно на каллезный характер язвы. Отличить доброкачественную язву желудка от злокачественной помогает эндоскопическое, цитологическое исследование, а также множественная биопсия с разных участков язвы.
Лечение. Острые и рецидивирующие язвы в стадии обострения лечатся, как правило, консервативным путем. Обычно для заживления язвы требуется от 4 до 8 нед, а при больших или застарелых язвах — и более длительный промежуток времени. Эндоскопический или рентгеноскопический контроль проводится через 8 нед и до полного заживления. Если полное заживление не наступает, проводится повторная биопсия.
При осложнениях язвы (пенетрация, перфорация, рубцовый стеноз, повторяющиеся кровотечения), отсутствии эффекта от консервативной терапии, частом рецидивировании неосложненной пептической язвы, лишающем больного трудоспособности, подозрении на злокачественную язву желудка показано хирургическое лечение.
Полипы и полипоз желудка. Полипы бывают гиперпластическими и аденоматозными.
Гиперпластические изменения встречаются в 80-90% случаев всех полипозных образований в желудке и относятся к опухолеподобным поражениям. В 10-20% случаев возникают аденоматозные полипы — доброкачественные эпителиальные опухоли. Обычно они имеют вид выступающих в просвет желудка округлых образований, расположенных на тонкой ножке или широком основании.
К числу предраковых относят железистые аденоматозные полипы. Дисплазия разной степени выраженности в аденоматозных полипах отмечается в 40-60% случаев, а дисплазия III степени — в 5-10%. Если гиперпластические полипы перерождаются в рак в 1-2% случаев, то плоская аденома — в 6-21%, а папилловирусная аденома — в 20-75% случаев;
Клиника. Одиночные полипы могут протекать бессимптомно и быть случайной находкой. Клинически они проявляются, как правило, при сопутствующем хроническом гастрите. При распаде опухоли возможны кровотечения, при ущемлении полипа — приступ боли в эпигастрии, тошнота, рвота.
Диагностика. Ведущая роль в распознавании полипоза и полипов желудка принадлежит рентгенологическому и гастроскопическому методам.
Биопсия при эндоскопии позволяет дать цитологическую и морфологическую характеристику полипов.
Лечение. Аденоматозные полипы лечат хирургически. При одиночных полипах возможна эндоскопическая полипэктомия, при множественных — выполняется резекция желудка или гастрэктомия.
Оперированные больные находятся под диспансерным наблюдением. Не реже одного раза в 6 мес проводится эндоскопическое исследование, также периодически комплексное лечение, включающее рациональную диету, витаминотерапию, седативные средства, санаторно-курортное лечение.
Пернициозная анемия (болезнь Аддисона) может быть определена как отсутствие внутреннего фактора Касла, связанное с полной атрофией слизистой оболочки фундального отдела желудка и потерей париетальных клеток. Болезнь диагностируется, когда отмечается полная атрофия слизистой оболочки фундального отдела желудка, как правило, это бывает после 50 лет. На момент обнаружения болезни воспаление в слизистой оболочке отсутствует, т. е. патологический процесс представляет собой атрофию без гастрита.
Некоторые данные указывают на иммунологическую и наследственную основу пернициозной анемии, называемой также гастритом типа А.
При этой болезни в 90% случаев в организме присутствуют антитела к париетальным клеткам желудка; а в 60% случаев — антитела к внутреннему фактору Касла (как блокирующие, так и связывающие его). Анемия обычно развивается постепенно и незаметно, прогрессируя по мере истощения запасов витамина В в печени.
Рак желудка при пернициозной анемии встречается в 0,5-12,5% случаев.
Больные с пернициозной анемией обычно наблюдаются у терапевта и гематолога. Для больных старше 50 лет обязательно эндоскопическое исследование желудка 1 раз в год.
Болезнь Менетрие — поражение желудка неизвестной этиологии, проявляющееся очень большими желудочными складками, большими железами с незначительным их воспалением и кистозным расширением; при этом изредка затрагивается подслизистый слой; часто процесс ограничивается телом и дном желудка (антральный отдел обычно не поражается). Иногда ширина и высота складок достигает 3,5 см. Характерно повышенное слизеобразование, гипосекреция соляной кислоты и пепсина, Уменьшение содержания сывороточных белков, приводящее к появлению гипоальбумических отеков.
Клиника. Характерны боль в эпигастрии, потеря массы тела, тошнота.
Течение заболевания хроническое (ремиссии, обострения), иногда наступает спонтанное выздоровление либо переход в атрофический гастрит.
Болезнь Менетрие, как правило, встречается в возрасте 30-60 лет.
Диагностика. При рентгенологическом и эндоскопическом исследовании выявляются очень крупные складки, которые никогда не переходят на пилорический отдел (показана биопсия на всю толщину складки). В 5-10% случаев развивается рак желудка.
Лечение — консервативное; в случае тяжелой гипоальбуминемии может быть необходимой резекция желудка.
Атрофический гастрит резецированного желудка. Закономерным исходом резекции желудка является развитие хронического гастрита в культе, который сопровождается дисплазией и кишечной метаплазией эпителия вследствие снижения кислотности желудочного сока и заброса желчи в культю желудка.
Рак культи желудка возникает у 0,4-7,8% больных из числа оперированных по поводу неопухолевых заболеваний желудка через 10, 15, 20 лет после операции.
Пациенты с резецированным желудком нуждаются в постоянном диспансерном наблюдении на протяжении всей жизни. Один раз в год им должно выполняться гастроскопическое обследование культи желудка.
Пролиферация покровно-ямочного эпителия: возможные причины, симптомы, проведение диагностики и лечение
Стенка желудка состоит из 4 слоев: внутренней слизистой оболочки, подслизистой основы, мышечного слоя и наружной серозной оболочки. Слизистая оболочка (СО) в норме складчатая, в ней имеются углубления – ямки, плоские участки (поля) и складочки.
Эпителий слизистой – высокопризматические (столбчатые) клетки, которые выстилают весь желудок и все его складки в один слой. Клетки этого эпителия секретируют особую слизь, она образует слой до 1-1,5 мм толщиной. При производстве ферментов и соляной кислоты в этом слое образуются временные каналы. Слизь защищает стенку от переваривания соком желудка и различных повреждений. Обновление эпителия происходит каждые 1-3 суток.
Что такое пролиферация
Клеточная пролиферация – это нормальный процесс, необходимый организму для обновления. Иначе говоря, это физиологическое размножение клеток с итогом в виде увеличения объема ткани. Управляется этот процесс гормонами. Пролиферация происходит в любом органе и ткани. Она контролирует состояние иммунитета, приводит к уничтожению дефектов тканей, регенерирует их и восстанавливает прежнее функционирование органов. За счет пролиферации растет соединительная ткань, формируются новые сосуды, рубцуются ожоги, устраняются повреждения с заменой тканей на новые клетки или соединительную ткань. Это касается клеток крови, эпителия и слизистых, хрящей, стенок миокарда и пр. Наиболее активный процесс происходит в слизистой желудка.
Но пролиферация при определенных условиях может становиться патологической, т. е. избыточной. Например, при повышенной концентрации соматропина она приводит к увеличению органов и конечностей. Если в процессе пролиферации нарушается дифференцировка клеток, это становится началом онкологии с появлением атипичных разрастаний. Такое бесконтрольное активное (аномальное) деление клеток называется гиперпролиферацией или гиперплазией. Это можно также объяснить преобладанием пролиферации над дифференциацией клеток слизистой. Тогда число узко дифференцированных клеток уменьшается и эпителий начинает терять свои «законные свойства» за счет незрелых клеток. Пролиферация покровного эпителия может и часто сопровождается процессами кишечной метаплазии желудка.
Гиперплазия
Пролиферация покровно-ямочного эпителия желудка является одним из подвидов пролиферации слизистой. Название дано потому, что в результате разрастания ткани происходит образование ямок штопорообразной формы. Данная пролиферация означает гиперплазию клеток, выpaбатывающих слизь (бокаловидные клетки), которая играет защитную роль. Покровный эпителий подвергается мутации, в клетках повышается содержание муцина, выталкивающего ядра к основанию клетки, патологические клетки начинают замещать здоровые. Формируются ямки в слизистой, которые по форме напоминают штифт штопора. Процесс является предвестником онкологии.
Чаще всего пролиферация покровно-ямочного эпителия возникает при гиперпластическом гастрите, язвенной болезни, язвенноподобном раке. По клинике и морфологии они идентичны, поэтому требуется биопсия. Цитологическое исследование может выявить выраженную пролиферацию покровно-ямочного эпителия желудка. По сути, это предраковое состояние, и такие больные должны находиться на учете у онколога и проходить систематическое обследование.
Причины развития
Главная причина – хроническое или длительное повреждение и раздражение слизистой, что вызывает появление ран и язв. Помимо вышеназванных патологий, причиной может быть:
Классификация
Выделено несколько типов желудочной гиперплазии. Они различаются по виду и поражаемым участкам. К основным относятся следующие:
Коротко о видах
Существуют следующие виды патологии:
То есть можно сказать, что пролиферация клеток покровно-ямочного эпителия это пролиферативный рост клеток, выpaбатывающих слизь.
Степени пролиферации
Сегодня гиперплазию разделяют на 3 этапа:
Симптомы и признаки
Долгое время человек не догадывается о существовании у себя патологии, у него нет никакого недомогания, поэтому так запаздывает ранняя диагностика. Затем, по мере прогрессирования процесса, сначала после еды появляется сильная боль в верхней части живота, тошнота, потеря аппетита, кислая отрыжка, икота.
В запущенных стадиях наблюдается рвота, общая слабость, вздутие живота, метеоризм. Боли могут носить схваткообразный характер — сначала они колющие или в виде жжения, затем становятся ноющими. Стул нарушается, склонен к диарее. Появляются признаки интоксикации – бледность, головная боль, головокружения, температура, чувство напряженных мышц. Симптомы неспецифичны, поэтому часто остаются без внимания. Ранняя диагностика имеет первостепенное значение: необходимо своевременно выявить и назначить эффективное лечение пролиферации покровно-ямочного эпителия желудка. Он опасен, но на первых стадиях податлив терапии.
Диагностические мероприятия
Главным методом диагностики является гастроскопия. При таком обследовании возможно проведение биопсии с последующей гистологией. Досконально осматривается слизистая желудка и все изменения в ней специалист может увидеть сразу.
При обследовании врач может увидеть новообразования, аномалию тканей и оболочек.
Рентгенография с барием позволит выявить полипы, их форму и размеры ножек. При установлении этиологии проводится анализ на наличие Хеликобактер пилори. Это и тест на дыхание с применением мочевины, и анализ крови на антитела.
Если поставлен диагноз «выраженная пролиферация покровно-ямочного эпителия hp» с некоторым количеством крестиков, то это говорит о присутствии в слизистой Хеликобактер пилори. Немалую роль может сыграть биопсия, ее проводят при гастроскопии. Исследование дает возможность установить факт наличия болезни и ее подвид. Надо сказать, что сочетание пролиферации покровно-ямочного эпителия и хеликобактера – не такое уж редкое явление.
Принципы лечения
Терапия заболевания многокомпонентная, имеет цель улучшить моторику желудка и нормализовать выработку соляной кислоты.
Лечение пролиферации покровно-ямочного эпителия, т. е. гиперпластического гастрита, зависит от этиологии, подвида пролиферации, гипо- или гиперацидности, тяжести клиники и сопутствующих заболеваний. Самостоятельное назначение препаратов категорически запрещено.
Как лечить пролиферацию покровно-ямочного эпителия желудка? Для терапии назначают группы следующих препаратов:
Народные методы лечения
Что касается народных способов лечения, то они могут помочь на начальных стадиях. Фитотерапия используется только по согласованию с лечащим врачом, носит симптоматический характер. Применяют отвары трав с противовоспалительным эффектом.
Очень полезной считается ромашка – чай из нее имеет спазмолитическое и противовоспалительное действие. Антибактериальными свойствами обладает имбирь. Чай с мятой, настой петрушки или иван-чая снимут тошноту и изжогу.
Когда нужна операция
Оперативное лечение гипертрофического гастрита проводят при неэффективности консервативной терапии. Показания к операции следующие:
Проводится эндоскопическое удаление полипов (полипэктомия), резекция желудка (полная или частичная). Полипы образуются при всех видах гиперплазий, могут быть и наследственными. Последние чаще злокачественные
Эндоскопически удаляют полипы больше 1 см. Маленькие образования не удаляют, если нет подозрения на злокачественность, но их развитие отслеживают – раз в полгода обследуют.
Специальная диета
Питание должно быть сбалансированным. Следует принимать пищу небольшими порциями (дробно), желательно в одно время, каждые 3 часа.
Желательно полностью отказаться от алкоголя и любых, раздражающих слизистую, продуктов: солений, копченостей, маринадов, консерваций, квашеных блюд, фастфудов, газировки и полуфабрикатов. Соль надо минимизировать, под запрет попадают консервы и красное мясо. Вся еда должна быть только отварной, все жареное под запретом.
Рекомендован стол № 2. Эта система питания назначается при болезнях кишечника и гастритах. Ее предназначение – остановить развитие воспаления и нормализовать работу секреторного аппарата желудка.
Прогноз зависти от подтипа гиперплазии и ее интенсивности, своевременности и современности диагностики.
Профилактические мероприятия
Специфической профилактики гиперплазии желудка не существует, но общие рекомендации по оздоровлению никто не отменял. Питание должно быть с достаточным содержанием витаминов и минералов, следует отказаться от курения и спиртного, избегать негативных эмоций и стрессов. Старайтесь выбирать продукты с наименьшим количеством консервантов и канцерогенов. Заведите привычку перед каждым приемом пищи выпивать стакан воды, чтобы за сутки в организм поступало не меньше 2 л чистой воды. Не злоупотрeбляйте противовоспалительными препаратами, даже если они вам помогают. Активный образ жизни тоже поможет избавиться от множества болезней. Не забывайте каждые полгода посещать гастроэнтеролога. Если вам очень не нравится метод ЭФГДС, можете просто пройти УЗД.
Пролиферация покровно-ямочного эпителия является опасной патологией, которая в запущенных случаях провоцирует онкологические заболевания. Важна ранняя диагностика, чтобы купировать очаги поражения на начальных стадиях.
Предраковые заболевания желудка: особенности цитологической диагностики
Предраковые заболевания служат фоном для развития в них злокачественных опухолей. Раннее выявление и своевременное лечение предраковых заболеваний стало неотъемлемой частью профилактики рака.
Для желудка такими заболеваниям являются:
В этой статье рассмотрены особенности цитологической диагностики данных заболеваний.
Хронический гастрит
В основе изменений при хроническом гастрите лежит сочетание дистрофических изменений железистых элементов, гипертрофических и атрофических изменений слизистой оболочки, воспалительной инфильтрации межуточной ткани и своеобразной перестройки желез.
Признаки покровно-ямочного эпителия
В цитологических препаратах при хроническом гастрите можно определить признаки пролиферации покровно-ямочного эпителия. В скоплениях и пластах клетки этого эпителия имеют кубическую форму, базально или центрально расположенное ядро и относительно широкую базофильную цитоплазму. Ядра клеток обычно отличаются некоторым полиморфизмом.
Отмечаются все переходы от зрелых, небольших размеров, интенсивно окрашенных ядер до относительно крупных светлых ядер с нежносетчатым рисунком хроматина. В отдельных группах могут встречаться клетки с признаками атипии в виде резкого укрупнения размеров клеток и их ядер, заметного увеличения ядерно-цитоплазматического отношения, появления неправильной формы ядер с нечеткими границами и неравномерным рисунком хроматина. Отмечается неправильное расположение и нагромождение ядер.
В случаях кишечной метаплазии в цитологических препаратах обнаруживаются высокие клетки цилиндрической, призматической или бокаловидной формы. Ядра этих клеток средних и крупных размеров, интенсивно окрашенные, располагаются в клетках эксцентрично. Цитоплазма у апикального края клетки более широкая и узкая, вытянутая у базального. Окрашивается она базофильно, а в апикальной части клетки и у ядра светлая, почти неокрашенная.
Эпителий желез в препаратах обычно обнаруживается в небольшом количестве. При хроническом атрофическом гастрите встречаются скопления дегенеративно измененных клеток железистого эпителия. Эти клетки имеют небольшие, гиперхромные, пикнотичные ядра и грубоволокнистую относительно широкую цитоплазму.
В материале, полученном при гастробиопсии, могут встречаться скопления лимфоидных элементов, которые попадают в исследуемый материал из собственного слоя слизистой оболочки. В этих скоплениях среди лимфоидных элементов различной степени зрелости обнаруживаются также ретикулярные, плазматические клетки и сегменто-ядерные нейтрофилы.
Полип желудка
Полип желудка (синонимы: аденома, фиброаденома, аденоматозный полип) считают доброкачественной опухолью, возникшей из покровно-ямочного эпителия. У больных полипозом желудка слизистая оболочка сохраняется интактной очень редко. Обычно наблюдаются изменения, характерные для атрофически-гиперпластического гастрита или гастрита “перестройки”.
В цитологических препаратах обнаруживается большое количество пластов и скоплений покровно-ямочного эпителия. При аденоматозных полипах встречаются также и железистоподобные структуры.
По сравнению с цитограммами при гастрите при этих заболеваниях отмечается некоторое преобладание молодых, незрелых клеток с укрупненными светлыми ядрами и нежносетчатым рисунком хроматина в них (См.рис). Встречаются единичные фигуры митозов.
Клетки эпителия желез и лимфоидные элементы обнаруживаются обычно в небольшом количестве. Судить о строении желез по цитологическим препаратам не представляется возможным. В случаях грануляционных полипов с обильными воспалительными инфильтратами в их строме в цитологические препараты могут попадать в значительном количестве нейтрофильные лейкоциты.
Хроническая язва желудка
Микроскопическое строение слизистой оболочки зависит от периода развития язвы желудка. В язвах прогрессирующих (период обострения) края и дно язвы бывают покрыты слоем экссудата, в который входит мукоидный секрет, фибрин, десквамированные клетки эпителия, лейкоциты и эритроциты. За слоем экссудата следует слой фибриноидного или набухающего некроза и затем грануляционная ткань.
Кроме фибробластов, гистиоцитов, плазматических клеток и лимфоцитов, в грануляционной ткани можно встретить нейтрофильные и эозинофильные лейкоциты, тучные клетки. При стихании процесса отмечается рубцевание грануляционной ткани и исчезновение некротических масс экссудата.
Непосредственно по краю хронической язвы слизистая оболочка желудка подвергается значительному утолщению за счет интенсивной пролиферации ямочного эпителия. Часто наблюдаются гиперпластические процессы и со стороны железистого аппарата.
В цитологических препаратах соответственно можно найти все упомянутые выше клеточные элементы.
В материале, полученном с краев хронической язвы, обычно обнаруживаются полиморфные, различной степени зрелости клетки покровно-ямочного эпителия. Преобладание незрелых крупных клеток с большими ядрами и базофильной цитоплазмой может свидетельствовать об интенсивной пролиферации эпителия.
В период обострения язвы в большом количестве встречаются дегенеративно измененные эпителиальные клетки без четких границ с укрупненными ядрами. Рисунок хроматина в них разреженный, в виде грубых волокон. В связи с большим клеточным распадом и явлениями цитолиза в материале, особенно полученном со дна язвы, можно видеть много „гoлых» ядер. В этих препаратах преобладают сегментоядерные лейкоциты и встречаются в значительном количестве элементы грануляционной ткани.
В период рубцевания язвы в мазки попадают очень полиморфные клетки гистиоцитарного типа, которые бывает трудно отличить от атипических эпителиальных клеток.
Лечение рака желудка в Израиле проводят специалисты мирового уровня которые практикуют новейшие методы борьбы с раком: химиотерапию, иммунотерапию и биотерапию с использованием новейших препаратов, которые подбираются индивидуально для каждого пациента в соответствии с результатами передовых молекулярно-генетических тестов, уникальную методику химиотерапии HIPEC, позволяющую добиться лучшего результата и избежать побочных эффектов, роботизированную хирургическую установку Да Винчи, с помощью которой проводятся микрохирургические операции повышенной сложности и многие другие. Узнайте подробнее заполнив заявку ниже.
Сложность диагностики по цитологическим данным
Изменения в составе и морфологии клеток слизистой оболочки желудка, которые наблюдаются при гастрите, полипозе и язве желудка, не являются строго специфическими и поэтому на основании только цитологических данных не представляется возможным диагностировать эти процессы.
Однако в гастроцитограммах при всех этих заболеваниях может определяться различная степень пролиферации покровно-ямочного эпителия.
В одних наблюдениях отмечается только незначительный полиморфизм эпителиальных клеток, в других явно преобладают незрелые, молодые элементы с некоторыми признаками их атипии. Описанные изменения вполне укладываются в понятие пролиферации эпителия, но в отдельных наблюдениях признаки атипии клеток настолько выражены, что трудно бывает с уверенностью исключить озлокачествление.
Чем опасна пролиферация кишечного эпителия
Пролиферация кишечного эпителия – это процесс роста и деления клеток, который может быть вызван причинами физиологического или патологического характера. Пролиферацию нельзя назвать заболеванием, это нормальное, естественное явление, которое необходимо для восстановления клеток и тканей. Но если деление клеток происходит чрезмерно интенсивно, это считается патологией и требует лечения.
Содержание
Что представляет собой пролиферация
Клетки и ткани железистого эпителия желудка систематически обновляются, поэтому пролиферация не останавливается. Она необходима для контроля уровня иммунитета, устранения имеющихся дефектов тканей, регенерации и восстановления их нормального функционирования.
Особенности питания после операции на желудке
На начальных этапах клеточный рост регенеративный, но со временем, при активном развитии слизистая перестает восстанавливаться. Поверхность эпителиальных желез покрывается неспецифическими клетками, имеющим вытянутую форму и темный цвет. В нормальном состоянии такие структурные элементы располагаются только в железистых шейках.
В случае если нарушается процесс клеточной дифференцировки, это приводит к возникновению обширных атипичных разрастаний. Состояние считается очень опасным, так как приводит к развитию онкологического заболевания – карциноме.
Пролиферация кишечного эпителия развивается на фоне травм и повреждений, а также заболеваний органов пищеварительного тракта.
Основные причины патологии:
Острая и хроническая форма язвы и гастрита приводят к повреждению слизистой кишечника и способствуют ускоренной пролиферации эпителия. Особенно часто процесс активизируется при утолщении слизистой, гиперплазиях, а также при полипах.
Симптомы заболевания
В большинстве случаев пролиферация кишечного эпителия выявляется случайно, при очередном медицинском осмотре. Патологический процесс не имеет ярко выраженных симптомов, поэтому диагностика чаще всего проводится уже на поздних, запущенных стадиях.
Все о том, как часто надо делать колоноскопию
При прогрессировании пролиферация вызывает следующие признаки:
Также у пациента наблюдается ухудшение общего самочувствия, его беспокоят слабость, хроническая усталость, сильные головные боли и головокружение, повышение температуры тела, бледность кожи и другие симптомы общей интоксикации организма.
Диагностика
При выявлении пролиферации кишечного эпителия необходимо выявить точную причину патологического процесса, после чего подбирается эффективная схема лечения. Основным диагностическим мероприятием считается гастроскопия, которая комбинируется с биопсией и дальнейшей гистологией взятого материала.
Также назначается рентгенография, которая помогает выявить полипы в полости пищеварительного тракта. Проводится исследование крови на наличие антител, анализ для определения Хеликобактер пилори.
Лечение пролиферации
Так как пролиферация не является самостоятельным заболеванием, а лишь симптомом другой патологии, назначаются лекарственные препараты для лечения основной болезни.
При гастрите, язве желудка или двенадцатиперстной кишки применяются средства для восстановления поврежденной слизистой пищеварительного тракта. Если же патологический процесс развивается на фоне воспаления, применяются противовирусные, антибактериальные и противовоспалительные препараты.
Назначаемые лекарственные препараты: