Прионы что это такое
Прионы: идеальные убийцы и возможный ключ к бессмертию
Фото: M24.ru/Евгения Смолянская
За свою историю человечество сталкивалось с огромным количеством войн, эпидемий, стихийных бедствий и других катаклизмов. В XXI веке, когда с эпидемиями, казалось, было покончено, у человечества появился новый вызов – прионы. Что это такое, чем они грозят людям и почему прионами так интересуются ученые всего мира – в материале M24.ru.
Ты помнишь, как все начиналось
В двадцатые годы прошлого столетия врачи столкнулись с новым и неизведанным доселе заболеванием. Немецкий невропатолог Ганс Герхард Крейтцфельдт наблюдал в своей клинике одну пациентку – 20-летнюю девушку. На начальной стадии болезни у нее была нарушена чувствительность в руках и ногах, быстро прогрессировали расстройства памяти, нервной деятельности, больная все чаще впадала в бессознательное состояние. Через несколько месяцев девушка умерла от расстройств дыхания и сердечной деятельности. Невропатолог, который в будущем станет видным нацистским врачом и будет принимать участие в программе «Эвтаназия», задокументировал ход болезни.
Спустя несколько месяцев доктор Альфонс Мария Якоб из Гамбурга столкнулся с тремя аналогичными пациентами. Молодые люди страдали от расстройств нервной деятельности, глотания, практически не осознавали происходящее вокруг и вскоре умерли. При вскрытии Якоб увидел интересное явление, которое раньше врачам наблюдать не приходилось, – поражен у больных был только мозг. Была зафиксирована массовая гибель клеток серого вещества головного мозга, а сохранившиеся нейроны отличались необычным набуханием. Ни в одном другом органе не было зафиксировано никаких патологических изменений. В память о двух первооткрывателях заболевание получило название болезни Крейтцфельдта – Якоба.
В те далекие годы вирусология как наука находилась еще в зачаточной стадии. Поэтому заболеванию было суждено долгое время оставаться в забвении. Этому поспособствовали Великая депрессия и Вторая мировая война. И лишь в пятидесятые годы прошлого века ученые начали активно интересоваться, что же все-таки происходит с людьми, которым не посчастливилось подхватить болезнь Крейтцфельдта – Якоба.
В то же время ученые открывают еще два заболевания, которые по своим симптомам и течению весьма и весьма напоминают описанный выше страшный недуг – куру и скрейпи. Первая болезнь была распространена среди народности форе на острове Папуа – Новая Гвинея, а вторым страдали овцы по всему миру. Но важным оказалось другое: симптомы болезней несколько отличались от болезни Крейтцфельдта – Якоба, но характер поражений был практически идентичен – образование пустот в тканях головного мозга и массовая гибель нервных клеток.
Казалось бы, все ясно. Имеется болезнь, ее вызывает какой-то вирус или бактерия, давайте разберемся, кто является возбудителем и устраним причину. Но не тут-то было! Все оказалось не так просто.
«Познавательные фильмы»: Вакцины
Исследования
Ученым удалось достаточно быстро установить, почему болеют папуасы. Выяснилось, что заболевают только те из них, кто участвовал в ритуальном поедании тел погибших от куру родственников. Согласно местным верованиям того времени, дети должны были обязательно отведать мозга умершего, считалось, что от этого у них прибавится ума. Неизвестно, прибавлялось ли у детей от этого ума, но все малолетние, участвовавшие в таких трапезах, обязательно оказывались зараженными куру.
Особенно масштабные исследования развернулись с агентом скрейпи. Для начала определили его размеры, они оказались стандартными для вирусов – 17–27 нанометров. После этого вирусологи всего мира стали разбираться в свойствах неизвестного возбудителя заболевания, и тут их ждали сюрпризы. Оказалось, что инфекционный агент совершенно невосприимчив к формалину, пепсину и трипсину, не реагирует на ферменты, разрушающие ДНК и РНК, устойчив к кипячению, ультрафиолетовому излучению и. проникающей радиации! С такими вирусами ученым сталкиваться еще не приходилось.
Фото: M24.ru/Александр Авилов
Больше того, возбудителя заболевания никак не удавалось увидеть в электронный микроскоп, что было уж совсем странно. В то время ученые уже умели распознавать вирусные частицы намного мельче, чем 17 нанометров, но вирус скрейпи (почесуха) так никто и не увидел – наблюдали лишь фрагменты клеточных мембран.
Еще одной интересной загадкой оказалось всякое отсутствие иммунного ответа организма больных. Организм людей, больных куру, и овец, страдавших от скрейпи, никак не реагировал на течение заболевания. При обычных болезнях, вроде гриппа и простуды, в организме увеличивается синтез интерферона (отвечает за иммунитет), что ведет к быстрому выпуску антител, которые соединяются с вирусными частицами и растворяют их. Ученые пытались обнаружить признаки хоть каких-либо антител, но потерпели неудачу.
Отчаявшиеся исследователи начали выдвигать гипотезы, что возбудителем является не вирус, а молекула полисахарида или же белка, но подтверждения эта версия так и не нашла. Ученые топтались на месте, пока в 1982 году американский невролог Стэнли Прузинер не заявил об открытии нового класса инфекционных агентов – прионах.
Что такое прион
До открытия прионов считалось, что болезни человека и животных могут вызываться исключительно живыми организмами или хотя бы вирусами, содержащими нуклеиновую кислоту. Однако все оказалось не так просто. Прион – это особый вид белка, который присутствует в любом человеческом организме.
Выяснилось, что либо под воздействием непонятных факторов, либо из-за мутаций в организме некоторых людей нормальный прионный белок, входящий в состав клеточных мембран, заменяется «неправильным». Второй вид прионного белка имеет другую структуру, вызывает гибель клеток, но самое интересное – способен самостоятельно размножаться (без каких-либо ДНК и РНК!) и менять нормальные прионы в соседних клетках на дефектные.
«Познавательный фильм»: Вирусы и защита от эпидемий
Таким образом, прионы оказались единственным видом инфекционных агентов, которых никак нельзя причислить к живым существам. Ведь, по своей сути, они не содержат никакой генетической информации и самостоятельно синтезируются организмом.
Естественно, исследователей заинтересовал самый главный вопрос – а зачем вообще в человеческом организме нужны прионы? В настоящее время известно уже достаточно много прионных болезней. Все они являются экстремально редкими, самая распространенная – болезнь Крейтцфельдта – Якоба – наблюдается у одного из миллиона человек. Также известно о синдроме Герстманна – Штраусслера – Шайнкера, фатальной семейной бессонице и куру. Некоторые исследователи включают в группу прионных заболеваний человека также болезнь Альперса у детей, амиотрофический лейкоспонгиоз (описан белорусскими учеными в конце прошлого века, болели работники одной из ферм) и спонгиоформный миозит (мышечное истощение).
Все эти заболевания являются смертельными, и лекарств от них пока не предложено. Но все же зачем организм синтезирует прионы? Какую он отводит роль для них?
Зачем нужны прионы?
В 70-е годы прошлого века два английских исследователя – Паттисон и Джебет – изучали на мышах действие вещества под названием купризон. В нормальных условиях оно связывает в организме ионы меди. Животным включили купризон в обязательную диету с целью посмотреть, какое действие он произведет на грызунов. И поразились! После 30 с лишним дней купризоновой диеты совершенно здоровые до этого мыши превратились в тяжелобольных. Причем все признаки заболевания полностью отвечали симптомами скрепи. Часть мышей, участвовавших в эксперименте, вскрыли и посмотрели – оказалось, что в головном мозгу животных произошли абсолютно те же изменения, что и при прионных болезнях.
Возник вопрос: а что если купризон мышам больше не давать? Попробовали – и через несколько дней грызуны выздоровели. Уже через 30 дней у них исчезли и вызванные купризоном изменения в мозговой ткани.
Спустя много лет было выяснено, что прионы весьма и весьма похожи на положительно заряженные частицы двухвалентной меди. И изменения, которые они вызывают в организме, практически идентичны. Таким образом, исследователи сделали вывод о том, что в нормальном состоянии прионы отвечают за оборот металлов, в частности меди. Но эти данные пока остаются лишь гипотезой.
Фото: ТАСС/Станислав Красильников
Еще одна группа американских исследователей принялась копать в другом направлении. Им удалось получить данные, что прионы помогают клеткам мозга прикрепляться друг к другу и участвуют в передаче сигналов внутри клетки. Это означает, что отсутствие прионов или их дефекты не позволяют клеткам мозга получать сигнал о других клеток, что ведет к развитию тяжелых нарушений в работе нервной и других систем организма.
Но самым интересным является предположение о том, что прионы участвуют в механизмах клеточного старения. Не секрет, что долгое время прионные болезни относили к группе старческих болезней, потому что вызываемые ими изменения весьма сходны с другими заболеваниями (вроде болезни Пика, Альцгеймера и других неврологических недугов). Наличие прионной инфекции как бы подталкивает организм к ускоренному старению. Естественно, это ставит очень важный вопрос: если лекарство от таких болезней будет найдено, не станет ли оно своеобразным ключом к долголетию или даже бессмертию организма? Но ответ на этот вопрос пока дать невозможно, поскольку функции прионов изучены еще недостаточно хорошо.
Способы заражения
В заключение поговорим о способах заражения. Их четыре. В первом и самом распространенном случае заболевание возникает как бы из ниоткуда. То есть жил себе человек, да вдруг взял и заболел. Этот путь возникновения болезни называется спорадическим и, кстати сказать, является наиболее распространенным. По нынешним представлениям, это происходит спонтанно под действием каких-то пока не установленных факторов.
Второй способ – наследственный. Некоторые виды болезней являются семейными и возникают из-за мутаций. В свою очередь, гены передаются потомству. Известно около 40 семей, страдающих фатальной бессоницей. Каждый десятый страдающий болезнью Крейтцфельдта – Якоба – страдает семейной формой этого заболевания.
Фото: M24.ru/Михаил Сипко
Третий способ – ятрогенный. Это означает, что заражение прионами произошло по вине медицинских работников при проведении каких-либо оперативных вмешательств. Однако описаны лишь несколько таких случаев, и все они произошло в 70-е годы прошлого века, когда о свойствах прионов еще никто не знал. Так, одна женщина заболела после того, как ей пересадили роговицу глаза от страдавшего болезнью Крейтцфельдта – Якоба мужчины.
А вот последний способ наиболее коварен и опасен. Дело в том, что человек восприимчив к прионам, которые поражают крупный рогатый скот. И при употреблении в пищу мяса больных животных заболевают и люди – у них развивается болезнь Крейтцфельдта – Якоба. В девяностые годы прошлого века настоящая эпидемия этого страдания разразилась в Англии.
Лечения пока нет. Однако ученые уже выяснили, что некоторые виды прионов разлагаются лишайниками, другим удалось описать особые антиприонные антитела (к инфекционным прионам).
Иными словами, перед исследователями стоит весьма непростая задача, которая не только поможет найти лекарство от тяжелых заболеваний, но и, возможно, поможет открыть секрет долголетия. Для этого нужно только одно – понять прионы.
Прионы: исследования таинственных молекул продолжаются
Путь прионов
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Прионные заболевания — феномен, открытый в двадцатом веке, и в нем же начавший играть большую роль: увеличение продолжительности жизни в развитых странах привело к тому, что все больше людей стало доживать до «своего Альцгеймера» или «своего Паркинсона». Природа нейродегенеративных заболеваний продолжает оставаться туманной, и ученые пока исследуют только отдельные их аспекты — например, причину развития именно в старческом возрасте или способность передаваться от одних видов живых существ другим.
«Био/мол/текст»-2012
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2012 в номинации «Лучшее новостное сообщение».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific.
Всё началось с того, что в 20 веке учёные заинтересовались природой необычных заболеваний человека и животных: куру, Крейтцфельда-Якоба, скрэпи. Заметное сходство патологии этих болезней дало основание для гипотезы об их инфекционности, что впоследствии было экспериментально подтверждено. Тогда возник вопрос о возбудителе данных заболеваний. Прежде чем был найден ответ, были выявлены необычайные свойства возбудителей: они не размножаются на искусственных питательных средах, устойчивы к высокой температуре, формальдегиду, различным видам излучений, действию нуклеаз. Очистка инфекционного материала и его изучение позволило провозгласить о том, что «во всём виноват» белок, который 30 лет назад получил название прион (от англ. pr[otenacious infect]ion — белковая инфекция).
Так, известные американские учёные — вирусолог и врач Д.К. Гайдушек, раскрывший инфекционную природу прионных болезней, в 1976 г. и биохимик С.Б. Прузинер, который определил прионы и разработал прионную теорию, в 1997 г., — были удостоены Нобелевских премий. Их работы стали импульсом для последующих исследований, благодаря которым были изучены новые виды прионных инфекций. Но, даже несмотря на неугасающий интерес к «прионной теме», образование прионов до сегодняшнего дня остаётся загадкой.
Биологическая сущность прионов
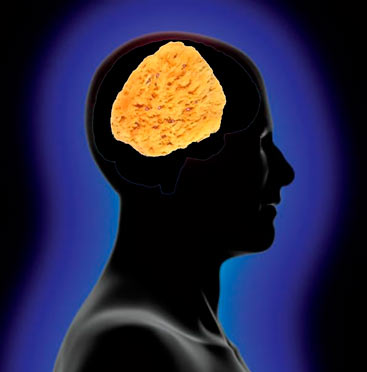
Рисунок 1. Метафора нейродегенеративного поражения мозга — это губка, в которую превращается нервная ткань в результате массовой гибели нейронов.
Существует упрощенное представление, что полимеризованные прионные фибриллы «протыкают» нейрон, что вызывает его гибель. На самом деле это не совсем так: предшествующие фибриллярной стадии сферические агрегаты прионов также обладают токсичностью (по крайней мере, для болезни Альцгеймера): «Альцгеймеровский нейротоксин: ядовиты не только фибриллы». — Ред.
Но как может нормальный природный белок (обозначается PrP C ) вдруг стать патологическим (PrP Sc ; Sc — от слова «scrapie»)? Что должно произойти? Как и в случае «обычной» инфекции, для такой трансформации необходима встреча с молекулой инфекционного приона. Существуют два пути передачи этой молекулы: наследственный (за счёт мутаций в гене, кодирующего белок) и инфекционный. То есть внедрение приона может произойти неожиданно — например, при употреблении в пищу недостаточно хорошо прожаренного или сваренного мяса (в котором должна присутствовать форма PrP Sc ), при переливании крови, при трансплантации органов и тканей, при введении гормонов гипофиза животного происхождения.
И тогда происходит удивительное событие: нормальные молекулы белка, контактируя с патологическими, сами превращаются в них, изменяя свою пространственную структуру (механизм трансформации остаётся загадкой и по сей день) [1]. Таким образом прион, как самый настоящий инфекционный агент, заражает нормальные молекулы, запуская цепную реакцию, разрушительную для клетки.
Некоторые сведения о прионах
Условия возникновения заболеваний
Условия возникновения прионовых болезней уникальны. Они могут формироваться по трём сценариям: как инфекционные, спорадические и наследственные поражения. В последнем варианте главную роль играет генетическая предрасположенность [2].
Знаменитый исследователь прионов Стэнли Прузинер (Stanley Prusiner) выделяет две поразительные особенности, присущие таким нейродегенеративным заболеваниям, как болезнь Крейтцфельда-Якоба, болезнь Альцгеймера и болезнь Паркинсона. Первая заключается в том, что более 80% случаев заболевания — спорадические (то есть, случайные, возникающие «сами собой»). Вторая: несмотря на то, что большое количество мутантных белков, специфичных к определённой болезни, экспрессируется в процессе зародышевого развития, формы наследования этих нейродегенеративных заболеваний проявляются позже. Это предполагает, что некоторые процессы происходят во время старения, которое «дает волю» болезнетворным белкам [5]. Более 20 лет назад автор утверждал, что данный процесс включает случайный рефолдинг (пересворачивание) белка в неправильно свёрнутый, что соответствует переходу в инфекционное состояние — прион.
Интересные факты насчет болезни Альцгеймера: ее вероятность может повышаться вследствие хронического недосыпания («Новый шаг к пониманию болезни Альцгеймера: возможно, недосыпание является одним из факторов риска»), а сам альцгеймеровский нейропептид (β-амилоид Aβ) может быть частью системы врожденного иммунитета («Возможно, β-амилоид болезни Альцгеймера — часть врождённого иммунитета»). — Ред.
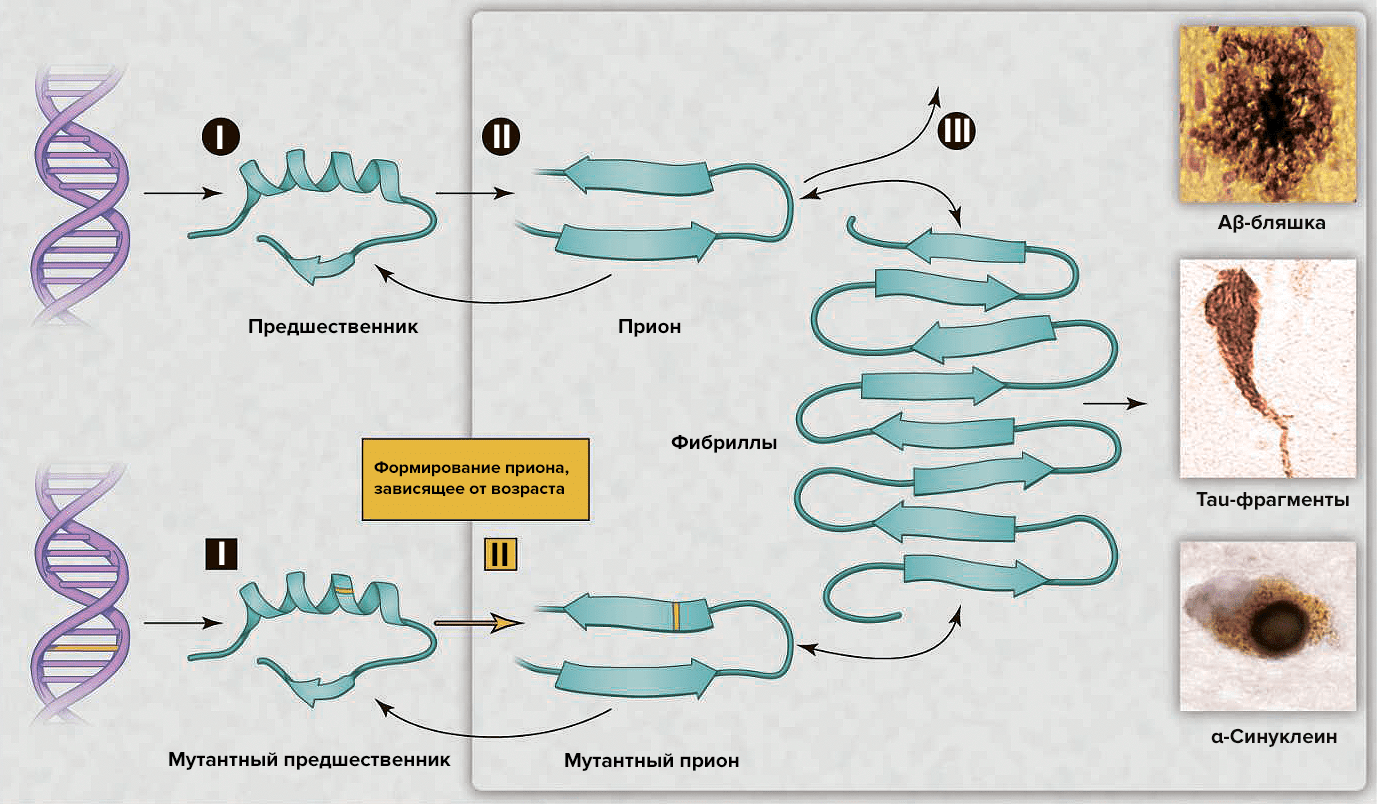
В последнее десятилетие интерес к этой теме возобновился в связи с возможностью развития диагностики и эффективной терапии [5]. Появилось множество различных объяснений для возрастных нейродегенеративных болезней, — например, окислительная модификация ДНК, липидов и/или белков; соматические мутации; измененный врождённый иммунитет; экзогенные токсины; несоответствия ДНК—РНК; нарушение работы шаперонов; отсутствие одного из аллелей гена [5]. Альтернативным комплексным разъяснением служит то, что различные группы белков могут формировать прионы. Несмотря на то, что небольшое количество прионов может быть удалено посредством путей белковой деградации, их чрезмерное накопление с течением времени позволяет прионам самостоятельно распространяться в организме (рис. 2), что приводит к нарушению деятельности центральной нервной системы [5].
Рисунок 2. Процессы нейродегенерации, вызванной прионами. Сверху: накопление «нормального» прионного белка повышает его вероятность перехода в токсичную конформацию, которая описывается бóльшим содержанием β-структуры. Прионы наиболее патогенны в форме олигомеров; после образования фибрилл токсичность снижается. В зависимости от того, о каком конкретно прионном белке идет речь, в патологическом состоянии он может образовывать бляшки, клубки или тельца включения. Возможные пути лекарственного вмешательства: (I) снижение концентрации «нормального» белка-предшественника; (II) ингибирование образования прионной формы; (III) уничтожение токсичных агрегатов. Снизу: Наследственная старческая нейродегенерация объясняется двумя событиями: наличием мутантной формы предшественника и образованием из него приона, готового к олиго- и полимеризации с образованием токсичных форм.
Группы риска прионных заболеваний
Вот кого прионные заболевания могут настичь с наибольшей вероятностью:
Лабораторная диагностика и лечение
Диагностика базируется на внутримозговом заражении мышат или хомяков, у которых медленно (до 150 дней) развивается соответствующее заболевание, если пациент был болен [2]. Часто проводится гистологическое исследование головного мозга погибших животных [2].
К сожалению, до настоящего времени еще не разработаны эффективные методы лечения прионовых болезней, хотя попытки предотвратить конформационный переход нормального белка в аномальный производятся. Поэтому самым надёжным способом предупреждения развития инфекционных форм является профилактика [2].
Особенно актуальным становится решение «прионного вопроса» в связи с нарастающей угрозой возникновения эпидемии через инвазивные медицинские операции и даже при приёме лекарственных средств.
Перспективы
По-видимому, интерес к прионам не угаснет до тех пор, пока предположения на их счёт полностью не подтвердятся и не будут найдены эффективные способы лечения прионных заболеваний. В статье [6] говорится о необходимости современного исследования, которое требует тщательного рассмотрения чужеродных прионов в экстраневрональных тканях.
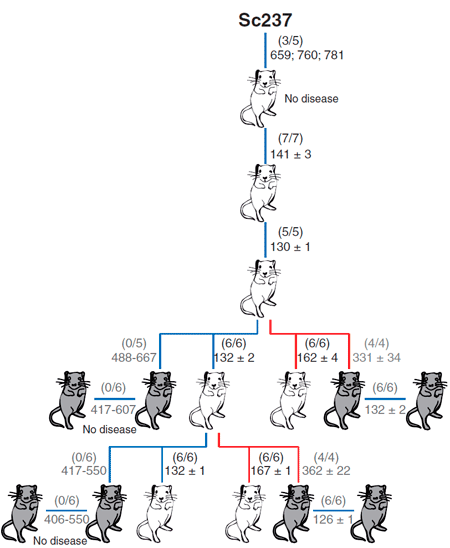
В качестве модельных объектов авторы использовали мышей: две линии, которые трансгенно экспрессировали овечий прионный белок, и одну линию, которая экспрессировала человеческий прионный белок (рис. 3). Задачей было сравнить эффективность межвидовой передачи инфекции посредством тканей мозга и селезёнки. Внутримозговое заражение чужеродным прионным белком выражалось в отсутствии или небольшом количестве инфекционного агента в мозгах этих мышей. Однако инфекционные чужеродные прионы обнаруживались в селезёнке на более ранних этапах заражения в сравнении с моментом, когда были использованы нейротропные прионы, тем самым определяя, что лимфатическая ткань может быть более пермиссивной к распространению чужеродных прионов по сравнению с мозгом.
Рисунок 3. Способность приона хомяков Sc237 заражать и передаваться при введении в мозг или селезенку трансгенным мышам, имеющим прионный белок PrP овцы (tg338; белые мыши) или человека (tg7; серые мыши). Число заболевших/инъецированных мышей показано в скобках; ниже приведено среднее время жизни (в днях).
Чем вызвана эта предпочтительная репликация прионов в лимфатических тканях, пока неизвестно. Однако полученные данные показывают, что человек может быть более чувствительным к чужеродным прионам, чем предполагалось ранее на основании присутствия прионов в мозгу, и по этой причине бессимптомный переносчик прионной болезни может быть не распознан. Это ещё раз подтверждает, что такая могущественная биомолекула как прион таит в себе немало загадок, раскрытие которых, возможно, поможет в понимании ряда неразрешимых проблем человечества.
Прионы: смертоносные молекулы-зомби

«Самое страшное в них то, что они действуют не как хищники, а как вирусы. Хищники по природе своей разумны и не уничтожают всех жертв поголовно. А они — просто размножаются, заражают и пожирают. Все остальное им совершенно безразлично», — так объясняет свой ужас перед зомби автор бестселлера «Мировая война Z» Макс Брукс. Но то же можно сказать и о прионах — настоящих смертоносных молекулах-зомби.
Сравнение с ходячими мертвецами напрашивается. Как и они, прионы в буквальном смысле слова разрушают мозг, превращая человека сперва в овощ, а затем — в труп. Как зомби из людей, так и они появляются из самых обычных белков. Их крайне сложно уничтожить, зато сами они смертельны в ста процентах случаев. Впрочем, трудно было бы ожидать иного от инфекционных агентов, которых вообще нельзя назвать живыми. Несколько столетий они ускользали от ученых — и даже потом в их существование поверили далеко не сразу. А теперь в них иногда видят даже источник жизни.
Овцы и людоеды
Первое «нашествие зомби» отмечено на рубеже XVII и XVIII веков, когда в Англии вовсю громыхала промышленная революция. Среди огромных стад, снабжавших шерстью быстрорастущие текстильные предприятия, то и дело стали попадаться «паршивые овцы». Напасть развивалась медленно, но неотвратимо: животные мучительно, до крови чесались об ограду, затем нарушалась координация движений, чаще и чаще случались судороги — через неделю-месяц все заканчивалось смертью.
Прошли столетия, Пастер описал бактериальные инфекции, а после работ Ивановского и Бейеринка появились представления и о вирусных заболеваниях. Но «почесуха овец», или скрейпи, оставалась загадкой. Все говорило о поражении мозга, ткани которого болезнь превращала в нечто, похожее на губку, изъеденную неровными порами. Но на вопрос о ее возбудителе специалистам оставалось лишь разводить руками: ни бактерий, ни вирусов найдено не было. Зато нашлись у скрейпи последователи.
Инкубационный период скрейпи может растянуться на годы. Но как только у животного начинают проявляться первые симптомы, можно быть уверенным, что через несколько недель наступит смерть
В одном и том же 1920 году, но независимо друг от друга, Ганс Крейтцфельдт и Альфонс Якоб описали неизлечимое и неумолимое поражение нервной системы человека. Возникая по неизвестной причине, обычно в пожилом возрасте, болезнь часто начиналась проблемами со сном и ослаблением когнитивных функций, развивалась потерей координации движений и деменцией, а несколько лет спустя венчалась параличом и функциональными нарушениями, окончательно несовместимыми с жизнью. Ткани мозга снова напоминали губку — и снова никаких следов возбудителя.
Редкое заболевание могло изучаться еще долго и неторопливо, не создавая особенного ажиотажа, если бы у него не обнаружился странный родственник в противоположной части света. В начале 1954 года чиновники Новой Гвинеи, тогда еще бывшей частью Австралии, составили отчет, в котором сообщали о вспышке диковинной местной болезни куру. «Первым признаком надвигающейся смерти становится слабоумие, за которым следует общая слабость вплоть до неспособности самостоятельно стоять на ногах, — говорилось в сообщении. — На следующем этапе жертва лежит, не в силах даже принять помощь, пока, наконец, не наступит гибель». Описанием болезни занялись медики Винсент Зигас и Карлтон Гайдушек, выяснившие, что поражает она лишь одно из новогвинейских племен, форе, выделяющееся среди соседей своим пристрастием к каннибализму. Вряд ли можно считать эту традицию какой-то особенно жестокой: существование в условиях серьезного дефицита жизненных ресурсов порождает и не такие обычаи. Так что после смерти аборигена форе его родственники поедали останки, причем по традиции мясо доставалось мужчинам, а женщины и дети довольствовались остальным, в том числе и мозгом. Как правило, заболевали именно они, причем мозг поражался в первую очередь: губчатая масса переродившейся нервной ткани была все той же, что и при скрейпи овец, и при болезни Крейтцфельдта — Якоба. Так что вскоре врачи решили, что имеют дело с медленной вирусной инфекцией, которая поражает нервную ткань и передается алиментарным путем (как «зомбированность»), через поедание больного мозга. Только вот выделить вирус снова никак не удавалось.
Коровы и радиация
Сходство болезней (необычно долгий инкубационный период и неизбежность летального исхода, заразность и, конечно, характерные перерождения нервной ткани мозга) позволило предположить у них и общую причину и объединить в группу трансмиссивных губчатых энцефалопатий.
» border=0 >
Инкубационный период у болезни Крейтцфельда — Якоба настолько длительный, что некоторые люди, получившие прионный белок еще во время вспышки «коровьего бешенства» 1980-х годов, лишь теперь начинают демонстрировать симптомы заболевания
Уже в 1960-х британские ученые предположили, что источником их может оказаться белок: таинственный инфекционный агент не инактивировался смертельной даже для вирусов дозой излучения. Это можно было объяснить крошечным размером его частиц, намного меньших, чем даже вирусы. Гипотеза показалась не лишенной смысла, хотя в корне противоречила «основной догме молекулярной биологии», которая постулировала однонаправленный поток информации, свойственный всему живому: от ДНК через РНК к белку. Возможно ли выбросить из этой короткой цепочки целых два звена — и сохранить многие свойства живого?
В 1970-е поисками возбудителя занялся калифорнийский невролог Стэнли Прузинер. Работа шла небыстро: используя биологические жидкости больных скрейпи овец, ученые подтвердили, что болезнь неумолима и развивается у всех до единой зараженных мышей, хотя инкубационный период затягивается на полгода, а то и дольше. Зато результаты многолетних экспериментов оказались сенсационными: снова и снова, выделяя прежде неуловимый инфекционный агент, ученые убеждались, что это «голый» белок.

Явление зомби
Было показано, что PrP С обладает высоким сродством с ионами меди, что может указывать на его возможную роль в удалении из клетки токсичных для нее тяжелых металлов. С другой стороны, максимальная концентрация PrP С наблюдается у контактов между нейронами некоторых областей мозга. Клеточные мембраны здесь буквально усеяны этим белком, что, возможно, говорит о том, что он играет какую-то роль в формировании или стабилизации синаптических контактов. Другая группа гипотез говорит о том, что PrP С необходим для удаления «загрязнений» с поверхности клеток. Связывая их, белок меняет форму, и, когда на мембране нейрона накопится достаточно много таких измененных белков, в нем запускается механизм уничтожения, а клетка гибнет.
«Существует, наверное, 20 или 30 гипотез о том, какую именно задачу может выполнять нормальная клеточная форма прионного белка. Но какой-то определенной, четкой функции у него не найдено, поэтому и возникают дебаты, — рассказал нам профессор Медицинской школы Мэриленда Илья Баскаков, не один год посвятивший изучению прионов и прионных болезней. — В последние годы активно обсуждается возможная роль PrP С в процессе развития нервной системы. Он может быть необходим для того, чтобы из стволовых клеток созревали новые нейроны — эксперименты показали, что, если у стволовой клетки выключен кодирующий этот белок ген PRNP, она не может превратиться в нервную».
Подобно зомби, ряды которых множатся с каждым укусом, инфекционная форма PrP Sc приводит к перерождению нормальных молекул PrP С в новые прионы — процесс развивается как автокаталитическая реакция, продукты которой сами ускоряют ее. Как и зомби, прионы любят «ходить» бесчисленными ордами: частицы PrP Sc складываются одна на другую стопками, образуя весьма устойчивые волокна, так что каждый конец такого образования становится центром притяжения для все новых и новых прионов.
Зомби по наследству
Болезнь Крейтцфельдта — Якоба, синдром Герстмана — Штраусслера — Шейнкера и другие прионные заболевания (а известно их уже несколько десятков) различаются не только характером поражения и течения, но и механизмами возникновения.
Считается, что одни из них чаще развиваются в результате спонтанного возникновения в клетке PrP Sc или получения его с пищей, а другие имеют генетическую природу.
Впервые «передача зомби по наследству» обнаружилась на рубеже 1970-х и 1980-х годов, когда настойчивый итальянский доктор Игнацио Ройтер провел собственное «расследование» смерти родственниц своей жены, умерших от крайне редкой причины — фатальной бессонницы. После смерти одного из родичей мозг его был изучен и обнаружена мутация в 178-й позиции гена PRNP. Неправильная, склонная к «прионному перерождению» конформация PrP С передается по наследству и обычно дает о себе знать уже в зрелом возрасте, когда человек начинает страдать от все более тяжелой бессонницы и угасает за считаные месяцы. Сегодня фатальная бессонница диагностирована в 40 семьях — приблизительно у сотни человек.
«По одиночке, мономерами, PrP Sc вообще не встречается, — говорит Илья Баскаков, — они существуют лишь в форме агрегатов-мультимеров. Показано, что самая маленькая частица PrP Sc может состоять примерно из шести мономеров, но, вырастая, они доходят до сотен и тысяч единиц». Достигнув больших размеров, белковое волокно разламывается на множество новых фибрилл, каждая из которых становится зародышем новой армии зомби-прионов. Подавленная скоплениями этих бляшек клетка гибнет, а PrP Sc распространяются дальше. Уничтожить их крайне непросто: эксперименты показали, что прионы невероятно устойчивы не только к радиации, но и к нагреванию, и даже к действию мощных клеточных ферментов-протеаз.
Обломки PrP Sc могут попадать в организм и извне, через биологические жидкости и ткани больных животных, во время некоторых медицинских процедур и просто с пищей. Большинство переродившихся белковых частиц, видимо, разрушается в желудочно-кишечном тракте, но некоторым удается добраться к месту действия, преодолев даже гемато-энцефалический барьер, стоящий на границе между кровью и тканями мозга. Способность PrP Sc проходить сквозь эту весьма надежную преграду остается одной из главных его загадок.
Добрые монстры
Такие свойства характерны не только для PrP С — даже у дрожжей найден свой «прионный белок» Ure2, способный переходить в нестандартную, но крайне устойчивую амилоидную форму. Возможно, это неспроста: «Прионы могут и не быть патогенными, — написал по этому поводу исследователь Рэндал Халфманн, — они могут играть роль „ненуклеиновой“, белковой наследственности у здоровых клеток и организмов». В подтверждение этой идеи Халфманн и его коллеги показали, что дрожжевой белок Ure2, приобретая нестандартную конформацию, влияет на целый ряд сигнальных путей клетки, в том числе и на активность гена FLO11. В свою очередь, синтезируемый на этом гене белок Flo11p необходим клеткам дрожжей для того, чтобы «сцепляться» друг с другом, формируя устойчивые к неблагоприятным условиям пленки. Так «прионное перерождение» белка Ure2 может способствовать адаптации и выживанию клеток.
Еще одну ложку меда к бочке прионного дегтя добавили работы Джеймса Чена и его коллег. Исследователи показали, что белок MAVS, один из необходимых для работы нашей иммунной системы, переходит в амилоидную прионную форму не во зло, а исключительно во благо. Обнаружив инфицированную определенными вирусами клетку, он «оседает» в ней, и его накопление служит сигналом к усиленному синтезу интерферонов и привлечению макрофагов для уничтожения зараженной клетки вместе со всем ее опасным содержимым.
На срезе участка мозга пациента с прионной болезнью амилоидные скопления белка видны как белые бляшки
«На этот счет существует интересная гипотеза, которая указывает на то, что такие амилоидные формы могут иметься вообще у всех белков, что это общее свойство полипептидных цепей, — продолжает Илья Баскаков. — Мало того, такие структуры наиболее стабильны. Поэтому высказано предположение о том, что именно в таких формах белки могли существовать в „пребиотическом супе“, в котором некогда проходила химическая эволюция молекул и зарождалась жизнь».
Действительно, некоторые эволюционисты полагают, что амилоидные конформации белков обладают всеми ключевыми способностями, необходимыми для роли «предков жизни». Они способны изменяться и размножаться, выполнять определенные функции, передавая свои особенности следующим поколениям. Если эта идея справедлива, то мы живем в очень странном мире, где все живое появилось на свет от странных и опасных белков, которые сегодня мы можем воспринимать не иначе как безжалостных зомби.