какие гормоны регулируют водно солевой обмен
Водно-электролитный обмен в организме здорового человека: принципы регуляции
Регуляция водно-солевого обмена, как и большинство физиологических регуляций, включает афферентное, центральное и эфферентное звенья. Афферентное звено представлено массой рецепторных аппаратов сосудистого русла, тканей и органов, воспринимающих сдвиги осмотического давления, объема жидкостей и их ионного состава. В результате, в центральной нервной системе создается интегрированная картина состояния водно-солевого баланса в организме. Так, при увеличении концентрации электролитов и уменьшении объема циркулирующей жидкости (гиповолемии) появляется чувство жажды, а при увеличении объема циркулирующей жидкости (гиперволемии) оно уменьшается. Следствием центрального анализа является изменение питьевого и пищевого поведения, перестройка работы желудочно-кишечного тракта и системы выделения (прежде всего функции почек), реализуемая через эфферентные звенья регуляции. Последние представлены нервными и, в большей мере, гормональными влияниями. Увеличение объема циркулирующей жидкости за счет повышенного содержания воды в крови (гидремия) может быть компенсаторным, возникающим, например, после массивной кровопотери. Гидремия с аутогемодиллюцией представляет собой один из механизмов восстановления соответствия объема циркулирующей жидкости емкости сосудистого русла. Патологическая гидремия является следствием нарушения водно-солевого обмена, например при почечной недостаточности и др. У здорового человека может развиться кратковременная физиологическая гидремия после приема больших количеств жидкости.
Гуморальная регуляция водно-электролитного баланса в организме осуществляется следующими гормонами:
— антидиуретический гормон (АДГ, вазопрессин), воздействует на собирательные трубочки и дистальные канальцы почек, увеличивая реабсорбцию воды;
— натриуретический гормон (предсердный натриуретический фактор, ПНФ, атриопептин), расширяет приносящие артериолы в почках, что увеличивает почечный кровоток, скорость фильтрации и экскрецию Na+; ингибирует выделение ренина, альдостерона и АДГ;
— ренин-ангиотензин-альдостероновая система стимулирует реабсорбцию Na+ в почках, что вызывает задержку NaCl в организме и повышает осмотическое давление плазмы, что определяет задержку выведения жидкости.
— паратиреоидный гормон увеличивает абсорбцию калия почками и кишечником и выведение фосфатов и увеличение реабсорбции кальция.
Содержание натрия и организме регулируется в основном почками под контролем ЦНС через специфические натриорецепторы. реагирующие на изменение содержания натрия в жидкостях тела, а также волюморецепторы и осморецепторы, реагирующие на изменение объема циркулирующей жидкости и осмотического давления внеклеточной жидкости соответственно. Содержание натрия в организме контролируется ренин-ангиотензинной системой, альдостероном, натрийуретическими факторами. При уменьшении содержания воды в организме и повышении осмотического давления крови усиливается секреция вазопрессина (антидиуретического гормона), который вызывает увеличение обратною всасывания воды в почечных канальцах. Увеличение задержки натрия почками вызывает альдостерон, а усиление выведения натрия — натрийуретические гормоны, или натрийуретические факторы (атриопептиды, простагландины, уабаинподобное вещество).
Состояние водно-солевого обмена в значительной степени определяет содержание ионов Cl- во внеклеточной жидкости. Из организма ионы хлора выводятся в основном с мочой, желудочным соком, потом. Количество экскретируемого хлорида натрия зависит от режима питания, активной реабсорбции натрия, состояния канальцевого аппарата почек, кислотно-щелочного состояния. Обмен хлора в организме пассивно связан с обменом натрия и регулируется теми же нейрогуморальными факторами. Обмен хлоридов тесно связан с обменом воды: уменьшение отеков, рассасывание транссудата, многократная рвота, повышенное потоотделение и др. сопровождаются увеличением выведения ионов хлора из организма.
Главные регуляторы обмена кальция и фосфора в организме: витамин D, паратгормон и кальцитонин. Витамин D (в результате преобразований в печени образуется витамин D3, в почках — кальцитриол) увеличивает всасывание кальция в пищеварительном тракте и транспорт кальция и фосфора к костям. Паратгормон выделяется при снижении уровня кальция в сыворотке крови, высокий же уровень кальция тормозит образование паратгормона. Паратгормон способствует повышению содержания кальция и снижению концентрации фосфора в сыворотке крови. Кальций резорбируется из костей, также увеличивается его всасывание в пищеварительном тракте, а фосфор удаляется из организма с мочой. Паратгормон также необходим для образования активной формы витамина D в почках. Увеличение уровня кальция в сыворотке крови способствует выработке кальцитонина. В противоположность паратгормону он вызывает накопление кальция в костях и снижает его уровень в сыворотке крови, уменьшая образование активной формы витамина D в почках. Увеличивает выделение фосфора с мочой и снижает его уровень в сыворотке крови.
Физиология эндокринной системы
Гормональные регуляторы водно-солевого обмена
Основными эффекторными регуляторами водно-солевого обмена являются альдостерон, натрийуретические пептиды и вазопрессин. Ангиотензин II участвует в этом процессе как стимулятор продукции альдостерона.
Стероидный гормон альдостерон, самый активный минералокортикоид, секретируемый клубочковой зоной коры надпочечников.
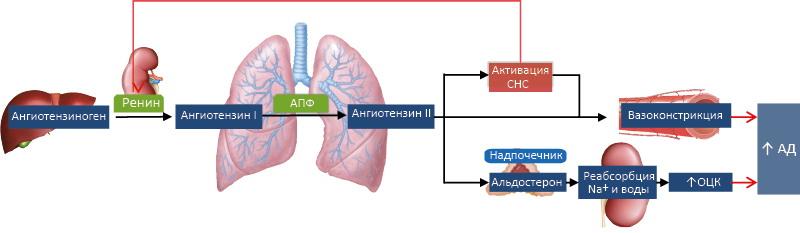
Продукция альдостерона регулируется ангиотензином II в процессе работы ренин-ангиотензин-альдостероновой системы (РААС). Прямые и обратные связи, регулирующие продукцию альдостерона, сложнее, чем в других гормональных осях, т.к. реализуются через объем крови и концентрации Na + и К + (Рис. 66).
Рис. 66. Ренин-Ангиотензин-Альдостероновая система (упрощённо).
АПФ – ангиотензинпревращающий фермент, ОЦК – объем циркулирующей крови
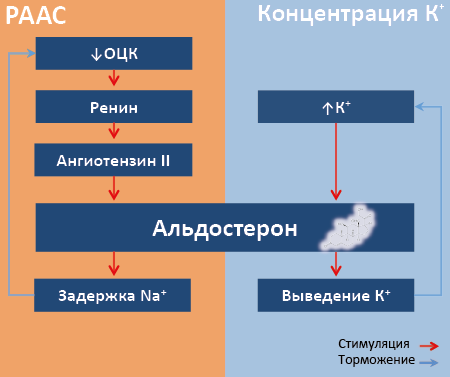
Рис. 67. Взаимосвязь активности РААС и концентраций ионов
Структура и механизм действия
Альдостерон – С21 стероид, относится к кортикостероидам, подгруппе минералокортикоидов.
Рецепторы минералкортикоидов относятся к семейству ядерных рецепторов и имеют практически одинаковое сродство к альдостерону и кортизолу. Клетки, несущие эти рецепторы, расположены в собирательных трубочках 107 коркового вещества почек, мозге и некоторых других орагнах. Избирательное действие альдостерона на почки достигается в результате инактивации кортизола под действием 11-бета-гидроксистероиддегидрогеназы 2 типа.
В настоящее время антагонисты РААС – наиболее применяемый класс антигипертензивных средств. Наиболее эффективны препараты, ослабляющие действие ангиотензина II, так как они не только снижают АД, но и предотвращают патологическую перестройку миокарда. Эффект антагонистов альдостерона не так выражен.
В клинической практике применяют:
• Ингибиторы ренина – Алискирен;
• Ингибиторы АПФ – напр. Эналаприл;
• Ингибиторы рецепторов AT1 – Валсартан;
• Антагонисты альдостерона – Эплеренон
Теоретически, наименьшим числом побочных эффектов должны были обладать ингибиторы ренина, благодаря полному отключению РААС (β1-адреноблокаторы также снижают выделение ренина). Однако на практике они уступали по эффективности ингибиторам АПФ, поэтому сейчас применяются только в комбинациях с другими антигипертензивными средствами.
Так как АПФ также инактивирует медиатор воспаления и вазодилататор брадикинин, на фоне применения ингибиторов АПФ может возникать сухой кашель. При появлении кашля вместо них назначают блокаторы рецепторов AT1, не обладающие таким побочным действием. Антагонисты альдостерона могут быть назначены при незначительном увеличении АД, или при снижении эффективности указанных выше средств (из-за «ускальзания альдостерона» – его синтеза альтернативными путями).
На системном уровне альдостерон вызывает:
Альдостерон влияет на ОЦК и АД через реабсорбцию Na + и Cl-. Чем она больше – тем меньше жидкости выделяется с мочой, и тем больше объём циркулирующей крови и артериальное давление. Клеточный механизм задержки Na + и выведения К + под действием альдостерона заключается в стимуляции экспрессии:
– Синтез вазодилататоров эндотелием (NO и PGI2).
Основная точка воздействия ангиотензина II на продукцию альдостерона – начальный этап его биосинтеза, превращение холестерина в прегненолон. В коре надпочечников ангиотензин II стимулирует пролиферацию клубочковой зоны и ее васкуляризацию.Помимо этого, ангиотензин II – вазоконстриктор и стимулятор секреции вазопрессина (видимо, за счет этого усиливает потребление воды). Продукция ангиотензина II снижается под действием вазопрессина и натрийуретических пептидов.
Н атрийуретические пептиды применяются при диагностике сердечной недостаточности. С этой целью измеряют концентрацию BNP в крови, так как его секреция желудочками прямо пропорциональна степени дисфункции сердца. Обычно измеряют концентрацию N-терминального фрагмента про-BNP (NTproBNP) т.к. он дольше живет в кровотоке. С диагностическими целями не используют ANP, так как его секреция увеличивается только на ранних этапах недостаточности, затем нормализуясь из-за истощения синтетической способности предсердий и их дилатации.
Н атрийуретические пептиды обладают гипотензивным эффектом, однако при гипертонической болезни их секреция может снижаться. Для увеличения активности эндогенных пептидов используют блокатор разрушающего их фермента – Омапатрилат.
В семейство натрийуретических пептидов входят предсердный натрийуретический пептид (ANP 110 ), мозговой натрийуретический пептид (BNP 111 ) и натрийуретический пептид типа C (CNP). ANP продуцируется преимущественно кардиомиоцитами предсердий в ответ на растяжение правого предсердия. Высвобождение BNP кардиомиоцитами происходит в ответ на постнагрузку (степень напряжения миокарда в систолу). CNP продуцируется эндотелиальными клетками и мозгом. Основной натрийуретический пептид в системном кровотоке – ANP.
Продукция ANP и BNP кардиомиоцитами усиливается не только в результате растяжения предсердия, но и под действием простагландинов, глюкокортикоидов, тиреоидных гормонов. Ангиотензин II и вазопрессин также увеличивают продукцию натрийуретических пептидов, уменьшая реабсорбцию воды и Na + в противовес действию альдостерона.
Структура и механизм действия
Все натрийуретические пептиды – небольшие пептиды, содержащие N-концевой и C-концевой фрагменты, соединённые внутренней аминокислотной петлёй. Петля образована дисульфидной связью и необходима для проявления биологической активности.
Натрийуретические пептиды передают сигнал через рецепторные гуанилатциклазы, преимущественно экпрессируемые почками и кровеносными сосудами. При связывании гормона с рецептором меняется конформация последнего. Это активирует гуанилатциклазную активность внутриклеточного домена рецептора, увеличивая продукцию цГМФ, который активирует цГМФ-зависимые протеинкиназы, фосфодиэстеразы и ионные каналы. Известно три типа рецепторов натрийуретических пептидов:
Основная функция клиренс-рецептора – связывание гормона и его удаление из кровотока.
Натрийуретические пептиды в почках:
– Снижают АД (вазодилятация + уменьшение ОЦК).
– Снижают активность симпатической НС.
Увеличение СКФ под действием натрийуретических пептидов обусловлено расширением приносящих и сужением выносящих артериол, что повышает фильтрационное давление в клубочке. Рост СКФ, в свою очередь, принимает участие в снижении ОЦК и АД (увеличенная экскреция Na + и воды) и замедлении почечного кровотока (спазм выносящей артериолы). Уменьшение АД под действием натрийуретических пептидов происходит также за счет системной вазодилятации 112 и торможению пролиферации гладкомышечных и эндотелиальных клеток сосудов.
Вазопрессин (антидиуретический гормон/АДГ)
Вазопрессин продуцируется крупноклеточными нейронами супраоптического и паравентрикулярного ядер гипоталамуса, транспортируется с помощью нейрофизина-2 вдоль аксонов в нейрогипофиз. В нейрогипофизе он накапливается и оттуда поступает в системный кровоток.
Секреция вазопрессина регулируется осмо- и барорецепторами, реагирующими на изменение ОЦК. Они стимулируют его секрецию при гиповолемии и гипотонии, а в противоположных ситуациях – снижают.Концентрация АДГ в крови повышается в экстремальных состояниях (кровопотеря, шок, стресс, травма и др.). Основные гормональные стимуляторы продукции вазопрессина – ангиотензин II и половые стероиды, а ингибиторы – натрийуретические пептиды и кортизол.
Структура и механизм действия
Вазопрессин представляет собой пептид из 9 аминокислот, структурно схожий с окситоцином, но отличающийся аминокислотами в 3 и 8 положениях.
Рецепторы вазопрессина – мембранные рецепторы, сопряжённые с G-белками. Разнообразные биологические эффекты вазопрессина опосредованы различными типами рецепторов: V1 (вазоконстрикция), V2 (антидиуретическое действие), V3 (секреция АКТГ гипофизом).
– Активация синтезированных аквапоринов.
– Повышение экспрессии гена AQP2.
Вазопрессин благодаря своему антидиуретическому действию поддерживает гомеостаз воды в организме, стимулируя её реабсорбцию в с обирательных трубочках почек. Это вызывает увеличение ОЦК, разведение плазмы крови (приводящее к гипонатриемии и снижению осмолярности), концентрирование мочи и уменьшение ее объема. Стимуляция реабсорбции воды в собирательных трубках возникает в результате действия АДГ через V2-рецептор на фосфорилирование аквапорина 2 (AQP2). Это служит сигналом для перемещения везикул с AQP2 к апикальной мембране клеток, где они формируют поры, проницаемые для воды.По мере восстановления изотоничности крови концентрация АДГ снижается, что служит сигналом к эндоцитозу AQP2. Однако в собирательных трубочках вазопрессин не только активирует уже действующие аквапорины, но и стимулирует синтез новых. Это происходит за счет АДГ-зависимого фосфорилирования транскрипционного фактора CREB, имеющего представительство в промоторе AQP2.
Помимо этого, вазопрессин способен: увеличивать АД, являясь мощным вазоконстриктором (через V1-рецептор) большинства регионарных артерий, артериол и микроциркуляторного русла; в аденогипофизе (через V3-рецепторы ) – стимулировать секрецию АКТГ; регулировать некоторые формы социального поведения, связанные с выхаживанием потомства (хотя и слабее окситоцина).
Д исфункция системы АДГ вызывает развитие несахарного диабета. Выделяют два типа несахарного диабета:
• Нейрогенный — нарушение секреции АДГ нейрогипофизом
• Нефрогенный — дисфункция V2-рецепторов.
Нейрогенный тип хорошо поддаётся заместительной терапии препаратами вазопрессина. Для уменьшения диуреза у пациентов с нефрогенным типом диабета используют тиазидные диуретики (ЛС Гидрохлортиазид и Хлорталидон), изменяющие ионный состав первичной мочи и, таким оразом, увеличивающие реабсорбцию жидкости.
1. Ball S.G. // Vasopressin and disorders of water balance: the physiology and pathophysiology of vasopressin.– Ann Clin Biochem.– 2007.– 44 (Pt 5):417-31.
3. Frohlich E.D. (auth.), Frohlich E.D., Re R.N. (eds.) // The Local Cardiac Renin-Angiotensin Aldosterone System. – 2009. – Springer US. – P. 184. – ISBN: 978-1-4419-0527-7, 978-1-4419-0528-4
4. Inga D. Neumann I.D., and Landgraf R. (Eds.) // Advances in Vasopressin and Oxytocin — From Genes to Behaviour to Disease. – 2008 Elsevier Science. – P. 608. – ISBN: 9780080932477, 9780444532015, 0444532013
5. Kalra A., Maharaj V., Goldsmith S.R.//Vasopressin receptor antagonists: from pivotal trials to current practice. – Curr Heart Fail Rep. – 2014. – 11 (1):10-8.
7. Luther J.M. // Aldosterone in vascular and metabolic dysfunction. – Curr Opin Nephrol Hypertens. – 2016. – 25 (1):16-21.
9. Mulatero P., Williams T.A., Monticone S., Viola A., Tizzani D. (auth.), Koch C.A., Chrousos G.P. (eds.) // Endocrine Hypertension: Underlying Mechanisms and Therapy / 2013.– Humana Press.– P. 318. – ISBN: 978-1-60761-547-7, 978-1-60761-548-4
10. Pandey K.N. // Endocytosis and Trafficking of Natriuretic Peptide Receptor-A: Potential Role of Short Sequence Motifs.– Membranes (Basel).– 2015.– 5 (3):253-87.
11. Theilig F., Wu Q. // ANP-induced signaling cascade and its implications in renal pathophysiology.– Am J Physiol Renal Physiol. – 2015. – 308 (10):F1047-55.
12. Volpe M., Carnovali M., Mastromarino V. // The natriuretic peptides system in the pathophysiology of heart failure: from molecular basis to treatment. – Clin Sci (Lond). – 2016.– 130 (2):57-77.
13. Whaley-Connell A., Johnson M.S., Sowers J.R. // Aldosterone: role in the cardiometabolic syndrome and resistant hypertension. – Prog Cardiovasc Dis. – 2010. – 52 (5):401-9.
105 Секреция ренина также стимулируется адреналином через β1-адренорецепторы.