Вся правда о гормонозаместительной терапии
Беру на себя смелость описать преимущества и страхи перед назначением гормонозаместительной терапии (ГЗТ). Уверяю вас – будет интересно!
ГЗТ у женщин сложнее и многограннее, чем у мужчин. Если мужчине нужен для замещения только тестостерон, то женщине и эстрогены, и прогестерон, и тестостерон, а иногда и тироксин.
При ГЗТ используются меньшие дозы гормонов, чем в препаратах гормональной контрацепции. Препараты ГЗТ не обладают контрацептивными свойствами.
Все приведённые ниже материалы основаны на результатах крупномасштабного клинического исследования ГЗТ у женщин: Womens Health Initiative (WHI) и опубликованы в 2012 году в консенсусе по гормонозаместительноной терапии НИИ Акушерства и гинекологии им. В.И. Кулакова (Москва).
Итак, основные постулаты ГЗТ.
Противопоказания к ГЗТ:
Обследования перед назначением ЗГТ:
О препаратах, используемых в ГЗТ.
Этрогены накожные (гели):
Дивигель 0.5 и 1 гр 0.1%, Эстрожель
Комбинированные препараты Э/Г для циклической терапии: Фемостон 2/10, 1/10, Климинорм, Дивина, Трисеквенс
Комбинированные препараты Э/Г для непрерывного приёма: Фемостон 1/2.5 конти, Фемостон 1/5, Анжелик, Клмодиен, Индивина, Паузогест, Климара, Прогинова, Паузогест, Овестин
Тиболон
Гестагены: Дюфастон, Утрожестан
Андрогены: Андрогель, Омнадрен-250
К альтернативным методам лечения относятся
растительные препараты: фитоэстрогены и фитогормоны. Данные о долговременной безопасности и эффективности этой терапии не достаточны.
В некоторых случаях возможно единовременное сочетание гормональной ГЗТ и фитоэстрогенов. (например, при недостаточном купировании приливов одним видом ГЗТ).
Женщины, получающие ЗГT, должны не реже одного раза в год посещать врача. Первое посещение намечается через 3 месяца от начала ГЗТ. Необходимые обследования для мониторирования ГЗТ врач вам назначит, учитывая особенности вашего здоровья!
Важно! Обращение администрации сайта о вопросах в блоге:
Уважаемые читатели! Создавая этот блог, мы ставили себе цель дать людям информацию по эндокринным проблемам, методам диагностики и лечения. А также по сопутствующим вопросам: питанию, физической активности, образу жизни. Его основная функция – просветительская.
В рамках блога в ответах на вопросы мы не можем оказывать полноценные врачебные консультации, это связано и недостатком информации о пациенте и с затратами времени врача, для того чтобы изучить каждый случай. В блоге возможны только ответы общего плана. Но мы понимаем, что не везде есть возможность проконсультироваться с эндокринологом по месту жительства, иногда важно получить еще одно врачебное мнение. Для таких ситуаций, когда нужно более глубокое погружение, изучение медицинских документов, у нас в центре есть формат платных заочных консультаций по медицинской документации.
Как это сделать? В прейскуранте нашего центра есть заочная консультация по медицинской документации, стоимостью 1200 руб. Если эта сумма вас устраивает, вы можете прислать на адрес patient@mc21.ru сканы медицинских документов, видеозапись, подробное описание, все то, что сочтете нужным по своей проблеме и вопросы, на которые хотите получить ответы. Врач посмотрит, можно ли по представленной информации дать полноценное заключение и рекомендации. Если да, вышлем реквизиты, вы оплатите, врач пришлет заключение. Если по предоставленным документам нельзя дать ответ, который можно было бы рассматривать как консультацию врача, мы пришлем письмо о том, что в данном случае заочные рекомендации или выводы невозможны, и оплату брать, естественно, не будем.
С уважением, администрация Медицинского центра «XXI век»
Вся правда о гормонозаместительной терапии
Беру на себя смелость описать преимущества и страхи перед назначением гормонозаместительной терапии (ГЗТ). Уверяю вас – будет интересно!
ГЗТ у женщин сложнее и многограннее, чем у мужчин. Если мужчине нужен для замещения только тестостерон, то женщине и эстрогены, и прогестерон, и тестостерон, а иногда и тироксин.
При ГЗТ используются меньшие дозы гормонов, чем в препаратах гормональной контрацепции. Препараты ГЗТ не обладают контрацептивными свойствами.
Все приведённые ниже материалы основаны на результатах крупномасштабного клинического исследования ГЗТ у женщин: Womens Health Initiative (WHI) и опубликованы в 2012 году в консенсусе по гормонозаместительноной терапии НИИ Акушерства и гинекологии им. В.И. Кулакова (Москва).
Итак, основные постулаты ГЗТ.
Противопоказания к ГЗТ:
Обследования перед назначением ЗГТ:
О препаратах, используемых в ГЗТ.
Этрогены накожные (гели):
Дивигель 0.5 и 1 гр 0.1%, Эстрожель
Комбинированные препараты Э/Г для циклической терапии: Фемостон 2/10, 1/10, Климинорм, Дивина, Трисеквенс
Комбинированные препараты Э/Г для непрерывного приёма: Фемостон 1/2.5 конти, Фемостон 1/5, Анжелик, Клмодиен, Индивина, Паузогест, Климара, Прогинова, Паузогест, Овестин
Тиболон
Гестагены: Дюфастон, Утрожестан
Андрогены: Андрогель, Омнадрен-250
К альтернативным методам лечения относятся
растительные препараты: фитоэстрогены и фитогормоны. Данные о долговременной безопасности и эффективности этой терапии не достаточны.
В некоторых случаях возможно единовременное сочетание гормональной ГЗТ и фитоэстрогенов. (например, при недостаточном купировании приливов одним видом ГЗТ).
Женщины, получающие ЗГT, должны не реже одного раза в год посещать врача. Первое посещение намечается через 3 месяца от начала ГЗТ. Необходимые обследования для мониторирования ГЗТ врач вам назначит, учитывая особенности вашего здоровья!
Важно! Обращение администрации сайта о вопросах в блоге:
Уважаемые читатели! Создавая этот блог, мы ставили себе цель дать людям информацию по эндокринным проблемам, методам диагностики и лечения. А также по сопутствующим вопросам: питанию, физической активности, образу жизни. Его основная функция – просветительская.
В рамках блога в ответах на вопросы мы не можем оказывать полноценные врачебные консультации, это связано и недостатком информации о пациенте и с затратами времени врача, для того чтобы изучить каждый случай. В блоге возможны только ответы общего плана. Но мы понимаем, что не везде есть возможность проконсультироваться с эндокринологом по месту жительства, иногда важно получить еще одно врачебное мнение. Для таких ситуаций, когда нужно более глубокое погружение, изучение медицинских документов, у нас в центре есть формат платных заочных консультаций по медицинской документации.
Как это сделать? В прейскуранте нашего центра есть заочная консультация по медицинской документации, стоимостью 1200 руб. Если эта сумма вас устраивает, вы можете прислать на адрес patient@mc21.ru сканы медицинских документов, видеозапись, подробное описание, все то, что сочтете нужным по своей проблеме и вопросы, на которые хотите получить ответы. Врач посмотрит, можно ли по представленной информации дать полноценное заключение и рекомендации. Если да, вышлем реквизиты, вы оплатите, врач пришлет заключение. Если по предоставленным документам нельзя дать ответ, который можно было бы рассматривать как консультацию врача, мы пришлем письмо о том, что в данном случае заочные рекомендации или выводы невозможны, и оплату брать, естественно, не будем.
С уважением, администрация Медицинского центра «XXI век»
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
Что же происходит с женским организмом в 45-55 лет?
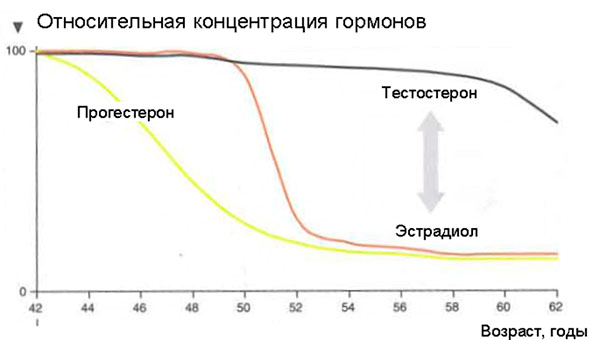
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
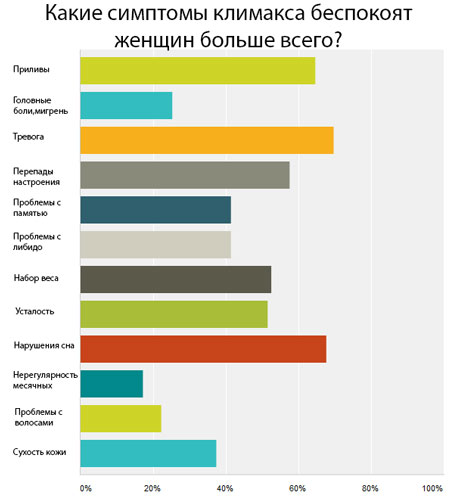
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
Препараты для монофазной терапии – когда месячные отсутствуют
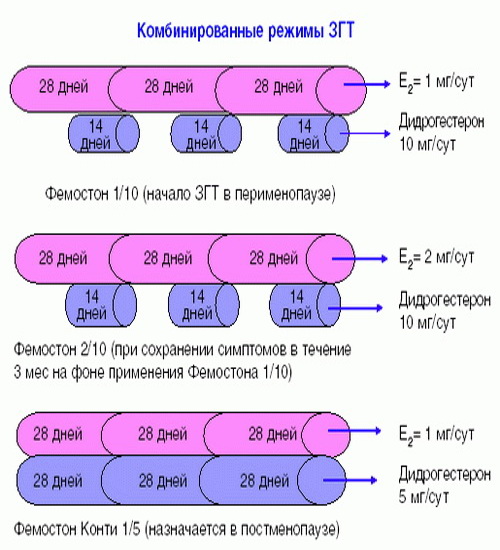
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
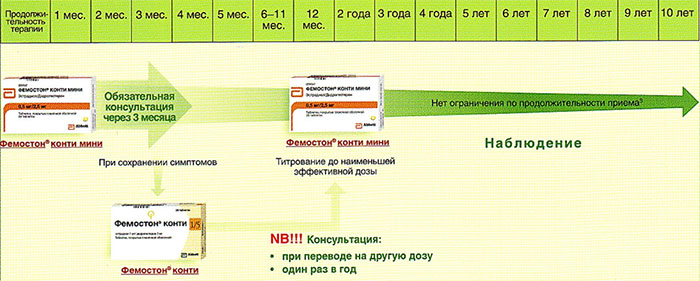
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
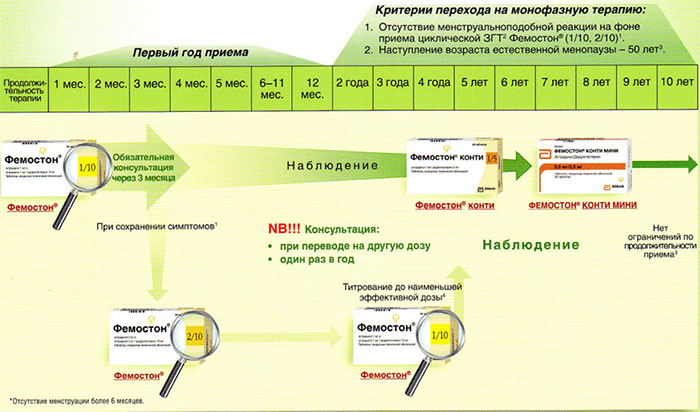
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).
Выбор оптимального препарата для заместительной гормональной терапии у женщин в перименопаузе и постменопаузе
Повышение качества жизни женщин в пери- и постменопаузе, профилактика сердечно-сосудистых заболеваний (ССЗ) и их осложнений, метаболических нарушений и остеопороза являются актуальными проблемами современной медицины во всех странах мира, независимо от уровня экономического развития. В настоящее время существует множество лекарственных и нелекарственных средств для коррекции менопаузальных осложнений, что значительно затрудняет выбор оптимального препарата, пути введения и режима дозирования. Однако гормонофобия, а также укоренившееся мнение о риске развития рака эндометрия и молочных желез на фоне приема заместительной гормональной терапии (ЗГТ) значительно ограничивают назначение эстроген-гестагенных препаратов, которые в отличие от биологически активных добавок, эффективность которых приравнивается к плацебо, могут значительно повысить и качество, и продолжительность жизни женщин в климактерии. За 13 лет в России не увеличилось количество женщин, получающих ЗГТ. Так, если в 1997 г., по данным В.П.Сметник, менее 1% женщин в России получали препараты ЗГТ, то в настоящее время официальных статистических данных нет, но если поделить количество всех продаваемых препаратов ЗГТ на количество женщин, нуждающихся в этих препаратах, то получится тот же неутешительный 1%, несмотря на то что в последнее время был пересмотрен ряд аспектов безопасности и эффективности ЗГТ.
Целью данного обзора литературы являлась оценка влияния разных компонентов, входящих в состав препаратов для ЗГТ, на сердечно-сосудистую систему, риск развития рака молочных желез (РМЖ) у женщин в климактерии, поскольку препаратов ЗГТ крайне много и они существенно отличаются по эффективности и безопасности.
Влияние ЗГТ на сердечно-сосудистую заболеваемость
Поскольку ССЗ являются основной причиной смертности женщин старше 50 лет, оценка влияния любых препаратов и особенно ЗГТ на сердечно-сосудистую систему является крайне важной. Однако в известных исследованиях, таких как HERS [1] (Heart and Estrogen/Progestin Replacement Study), WHI [2, 3] (Women’s Health Initiative) и WISDOM [4] (Women’s International Study of long Duration OESTROGEN after Menopause), направленных на оценку отдаленных результатов ЗГТ, был доказан ранее предполагаемый кардиопротективный эффект экзогенных эстрогенов (конъюгированных эквинных эстрогенов – КЭЭ). Более того, исследование WHI, предпринятое с целью изучения эффективности эстроген-гестагенной терапии в профилактике болезни сердца и переломов шейки бедра, а также определения риска развития РМЖ и толстого кишечника, связанного с гормональным лечением, было досрочно прекращено в связи с повышением риска инвазивного рака груди и получением данных, свидетельствующих о том, что в целом риск, связанный с лечением, превышает пользу от него.
Однако в многочисленных исследованиях показана кардиопротективная роль эндогенных эстрогенов в отношении ряда органов и систем, в том числе и сердечно-сосудистой системы, как у приматов, так и у людей.
В исследовании WHI [5] при общем повышении сердечно-сосудистых событий на фоне ЗГТ (средний возраст женщин, включенных в исследование, – 63 года) показано снижение сердечно-сосудистого риска у женщин в возрастной группе 50–60 лет, что наглядно демонстрирует необходимость более раннего назначения препаратов ЗГТ.
Основной целью исследования WHI была оценка пользы и риска от применения наиболее распространенного в США режима комбинированной гормонотерапии. При этом в первую очередь оценивали эффект лечения с точки зрения предупреждения ишемической болезни сердца. План исследования разрабатывали в 1991–1992 гг., набор участниц начали в 1993 г. Всего были отобраны 16 608 женщин в возрасте от 50 до 79 лет с интактной маткой, согласившихся на участие в исследовании. Отбор проводили в 40 клинических центрах на территории США. Участницы принимали либо конъюгированные эстрогены (КЭ) по 0,625 мг в сочетании с медроксипрогестероном ацетатом (МПА) по 2,5 мг ежедневно по непрерывной схеме (8506 женщин) либо плацебо (8102 женщины). Через некоторое время значительное число женщин перестали принимать лекарственные препараты (42% – в группе КЭ/МПА и 38% – в группе плацебо). Третью группу испытуемых составили 10 739 женщин с удаленной маткой, которые принимали только КЭ по 0,625 мг (без прогестина). Несмотря на то что план исследования разрабатывали видные специалисты в области статистики, эпидемиологии и клинических исследований, критериям отбора испытуемых не было уделено должного внимания. В результате выборка не была в достаточной степени репрезентативной и не соответствовала тому контингенту женщин, для которых обычно рассматривается возможность назначения ЗГТ. Авторы WHI сообщают, что в исследование включали «здоровых женщин в постменопаузе». Однако при включении в исследование не учитывались такие показатели, как наличие тяжелой гипертонии с артериальным давлением выше 200/105 мм рт. ст., перенесенные ранее переломы, связанные с остеопорозом, РМЖ в анализе, включая локализованные и инвазивные формы рака или маммограммы с отклонениями от нормы, а также проявления ССЗ ранее чем за 6 мес до начала исследования. Возраст испытуемых варьировал от 50 до 79 лет (в среднем 63,3 года; 33% – в возрасте 50–59 лет, 45% – в возрасте 60–69 лет, 21% – в возрасте 70–79 лет). Таким образом, 66% участниц были старше 60 лет и 21% старше 70 лет. При этом 2/3 из них гормональная терапия была назначена впервые. Такой сдвиг в сторону пожилых женщин, впервые принимающих препараты половых гормонов, при отборе испытуемых ведет к искажению результатов и занижению положительных эффектов ЗГТ в связи с увеличением частоты возрастных сердечно-сосудистых, тромбоэмболических и неопластических отклонений. В относительно большой популяции женщин такого возрастного состава наиболее вероятен атеросклероз. Данные исследования подтверждают это предположение. Действительно, инфаркт миокарда отмечен в анамнезе у 1,7%, инсульт– у 0,8%, тромбоэмболические явления – у 0,9%, шунтирование коронарной артерии и чрескожная коронарная реваскуляризация – у 1,3%, транзиторные ишемические приступы – у 2,8%, диабет – у 4,4%, гипертония – у 36%, гиперхолистеринемия – у 12,7% случаев. Всего 6,9% женщин принимали статины и 19% ацетилсалициловую кислоту.
В опытах на приматах продемонстрировано, что эстрогены через некоторое время после развития эстрогенного дефицита теряли свой защитный эффект, а при наличии атеросклеротических изменений сосудов способствовали увеличению сердечно-сосудистых событий [6, 7]. Поэтому обсуждение влияние ЗГТ на сердечно-сосудистые события должно включать и обсуждение оптимального времени назначения данных препаратов и индивидуальный подход к их выбору. Очевидно, что ЗГТ должна быть начата во время менопаузального перехода [6, 8, 9], поскольку есть основания полагать, что эстрогены эффективны для профилактики коронарной болезни сердца только тогда, когда лечение начато до появления признаков прогрессирующего атеросклероза. На это указывалось в ходе объединенного семинара по ССЗ и заместительной гормонотерапии Международного общества по проблемам менопаузы. Исследования, проводившиеся с участием женщин в постменопаузе с гиперхолестеринемией, показали, что эстрадиол в дозе 1 мг (без гестагенов) предупреждает развитие атеросклероза в той же степени, что и статины.
Несмотря на переоценку главных критических замечаний WHI [10–12], нельзя отрицать, что стандартные дозы эстрогенов действительно увеличивают риск развития тромботических осложнений, главным образом в течение 1-го года применения ЗГТ [13]. Частота инсульта также выше у женщин старших возрастных групп [3, 14, 15]. Однако в датском исследовании Danish Nurse Study отмечено, что увеличенный риск инсульта очевиден только у женщин в климактерии с гипертонической болезнью (при этом риск не повышался у женщин с нормальным артериальным давлением) и получавших эстроген-гестагенную терапию, в которой в качестве гестагенного компонента использовался норэтистерона ацетат [16]. В систематическом обзоре и метаанализе Magliano и соавт. показано, что ЗГТ не повышает риск смертности от ишемической болезни сердца и инфаркта миокарда [17]. Поскольку риск инсульта повышается с возрастом и при наличии гипертонии, необходимо учитывать, что у большинства пациенток в исследованиях WHI была нелеченая гипертензия [18]. Распространенность артериальной гипертензии у женщин в климактерии увеличивается приблизительно с 35% во время менопаузального перехода до 75% к 75-летнему возрасту [19]. Дефицит эстрогенов и снижение эластичности стенок артерий вероятно способствует возрастному прогрессивному увеличению систолического кровяного давления и в конечном счете к вероятности развивающейся гипертензии [20]. Кроме того, менопауза связана с повышением активности симпатической нервной системы [21] и активацией системы ренин–ангиотензин. В сочетании с другими факторами, такими как ожирение и оксидативный стресс, это может способствовать высокой распространенности гипертонии у женщин в пери- и постменопаузе.
Большое влияние на сердечно-соcудистую систему имеет гестагенный компонент, входящий в состав ЗГТ. Исследования на приматах показали, что МПА может ослабить защитное антиатерогенное действие эстрогенов и их благоприятный эффект на вазодилатацию. Частично это может объясняться глюкокортикоидным эффектом МПА, в результате которого активизируются рецепторы тромбина в стенках артерий.
Натуральный прогестерон обладает слабой антиминералокортикоидной активностью. В исследовании PEPI (Postmenopausal Estrogen/Progestin Interventions) отмечено увеличение артериального давления у женщин, получавших КЭЭ в сочетании с МПА уже в течение 1-го года применения, в то время как у пациенток, получавших КЭЭ в сочетании с микронизированным прогестероном, повышения артериального давления не отмечалось. Другой гестаген, не оказывающий негативного влияния на артериальное давление, – дидрогестерон, являющийся D-изомером прогестерона и не обладающий эстрогенными и андрогенными свойствами. Дидрогестерон, входящий только в препарат Фемостон®, является абсолютно метаболически нейтральным гестагеном, в связи с чем данный препарат не оказывает негативного влияния на метаболические показатели и сердечно-сосудистую систему. Более того, показано его позитивное влияние на все компоненты метаболическиго синдрома – ожирение, артериальную гипертензию, дислипидемию и нарушение углеводного обмена. Несмотря на сходство с эндогенным прогестероном по молекулярной структуре и фармакологическим свойствам, дидрогестерон эффективен в более низких дозах при пероральном применении по сравнению с прогестероном.
Половые гормоны и менопаузальный метаболический синдром
Метаболический синдром и сахарный диабет – главные факторы риска развития сердечно-сосудистых осложнений, особенно в сочетании с артериальной гипертензией. Частота сахарного диабета увеличивается с возрастом и в период менопаузы. Дефицит эстрогенов, возникающий в перименопаузе, в сочетании с абдоминальным ожирением и инсулинорезистентностью является одним из факторов риска развития сахарного диабета у женщин. В 2006 г. в метаанализе, основанном на 107 исследованиях, показано, что ЗГТ способствует уменьшению выраженности абдоминального ожирения, инсулинорезистентности, благоприятно влияет на липидный профиль и уменьшает число эпизодов впервые выявленного сахарного диабета [23]. У относительно здоровых женщин в пери- и постменопаузе, получающих КЭЭ, ни пероральный, ни трансдермальный эстрадиол существенно не влиял на уровень глюкозы. Однако отмечено разное действие КЭЭ и эстрадиола (перорального и трансдермального) на чувствительность к инсулину: в то время как при назначении эстрадиола отмечалось увеличение чувствительности, КЭЭ ее уменьшали [24]. Прогестины оказывают влияние на углеводный обмен и инсулинорезистентность, однако их влияние зависит как от способа введения прогестина, так и от его типа. Такие прогестины, как МПА и норэтистерона ацетат, могут негативно влиять на углеводный обмен и усугублять инсулинорезистентность. Напротив, прогестерон и дидрогестерон не оказывают негативного влияния [24], поэтому препараты, в состав которых входит дидрогестерон (Фемостон®), следует назначать женщинам с ожирением, инсулинорезистентностью, метаболическим синдромом и сахарным диабетом, а также тем, кому показана длительная ЗГТ.
Половые гормоны и функция эндотелия
Эндотелиальная дисфункция является фактором риска гипертонии. Нарушение функционального состояния клеток эндотелия ассоциируется с нарушением вазодилатации и считается предиктором последующих сердечно-сосудистых осложнений. Эндотелиальная дисфункция как ранняя фаза атеросклеротической дегенерации сосудов характеризуется нарушением синтеза NO и экспрессией на клеточной мембране адгезивных молекул. В ряде исследований отмечено, что прогестерон и МПА по-разному влияют на этот процесс. Прогестерон in vitro стимулирует транскрипционными и нетранскрипционными путями синтез NO в клетках эндотелия. Кроме того, при добавлении эстрадиола, натуральный прогестерон не уменьшал активности NO-синтазы или даже потенцировал эффекты эстрадиола. В отличие от этого МПА не способствовал синтезу NO и ухудшал вазодилатацию, вызванную эстрадиолом [26]. JY-P.Ho и соавт. [27] показали, что эндотелийнезависимая вазодилатация плечевой артерии также значительно увеличивается (от 5,9 до 13,9%) после трансдермального и перорального эстрадиола (6,0–14,7%) у здоровых женщин в климактерии. Нормальное состояние эндотелия – залог нормального функционирования сердечно-сосудистой системы. Эстрогены сохраняют функцию эндотелия in vitro и in vivo. Однако добавление синтетических прогестинов, таких как МПА, может снижать вазодилатирующий эффект эстрогенов [28–30]. Sorensen и соавт. показали, что норэтистерона ацетат уменьшал благоприятный эффект перорального эстрадиола на эндотелийнезависимую вазодилатацию [31]. Также отмечено, что МПА ухудшал вызванную эстрогенами вазодилатацию коронарных артерий [32] и эндотелийзависимую вазодилатацию плечевой артерии [33, 34]. В то же время показано, что дидрогестерон в качестве монотерапии или в сочетании с эстрадиолом обладал нейтральным эффектом на функцию синтеза NO клетками эндотелия, тогда как его устойчивый метаболит – дигидродидрогестерон увеличивал синтез NO, так же как и натуральный прогестерон [35].
ЗГТ и РМЖ
Влияние эстрогенов и их комбинации с прогестинами на молочные железы у женщин в постменопаузе представляет особый интерес. Эстрогены, как полагают, играют главную роль в развитии быстрого увеличения как нормального, так и злокачественного эпителия молочных желез [36]. Прогестерон также оказывает действие на пролиферативные процессы, хотя его роль еще изучена недостаточно. Влияние эстрогенов и прогестерона на рост эпителия молочных желез остается предметом дискуссии. Ассоциация между РМЖ и эстрогенами отмечена в эпидемиологических, клинических и экспериментальных данных, хотя существует много противоречий [37]. Так, если эстрогены приводят к развитию РМЖ, то почему частота РМЖ увеличивается у женщин в постменопаузе, несмотря на то что уровень эстрогенов в этот период драматически снижается? Таким образом, половые гормоны возможно и усугубляют течение РМЖ, но, скорее всего, не определяют их развитие, которое происходит прежде всего из-за накопления большого количества мутаций и хромосомных отклонений [38] и является генетически обусловленным.
Эпидемиология РМЖ в исследованиях у женщин в постменопаузе, получающих ЗГТ
Исследования HERS и WHI, которые считаются «золотым стандартом», показали, что сочетанное применение КЭЭ и МПА приводило к незначительному увеличению риска развития агрессивного РМЖ. Так, в исследовании WHI прирост увеличения риска РМЖ составил 8 случаев на 10 тыс. женщин ежегодно. В связи с чем публикация предварительных результатов этого исследования в 2002 г. привела к скандальным заявлениям в прессе, что заставило многих женщин отказаться от приема ЗГТ или не начинать его, хотя ни в одном из этих исследований не сообщалось об увеличении смертности от РМЖ [40]. Необходимо отметить, что в исследовании WHI у 16% женщин в семейном анамнезе был РМЖ, а 10% никогда не рожали – у таких женщин риск РМЖ был крайне высоким.
В исследованиях ЕЕ/ЕЕ II (6,8 года) повышение риска развития РМЖ было статистически недостоверным [39]. Учитывая последовательность развития РМЖ от carcinoma in citu до агрессивного рака, на фоне ЗГТ теоретически должно было бы увеличиваться число новых случаев злокачественных новообразований. Однако даже с начальных публикаций итогов WHI было очевидно, что количество случаев РМЖ у женщин, ранее не получавших ЗГТ, на фоне ЗГТ не увеличивалось. Подробный анализ показал, что за 5,6 года исследования значительно увеличивался риск РМЖ только у ранее получавших ЗГТ [41].
Влияние типа прогестина на развитие РМЖ
В группе эстроген + прогестин (КЭЭ+МПА) в исследовании WHI наблюдали увеличение случаев агрессивного РМЖ, в то время как у получавших только эстрогены уровень заболеваемости снижался. Хотя эти две группы были не совсем сопоставимы, это навело исследователей на мысль, что причиной такого различия может быть применение МПА. Как было показано Kenemans, добавление к эстрогену MPA или андрогенного, полученного из тестостерона, прогестина действительно немного увеличивало риск развития РМЖ [44]. По данным Schairer и соавт. [45], увеличенный риск РМЖ отмечался главным образом у худощавых пациенток (BMI
Кафедра эндокринологии была основана в 2008 году на Факультете повышения квалификации медицинских работников Российского Университета Дружбы Народов.