Благородные газы: что это?
Благородные (или инертные) газы – группа химических элементов, обладающих схожими свойствами. Что они из себя представляют и в чем заключается их особенность, мы расскажем вам в этом материале.
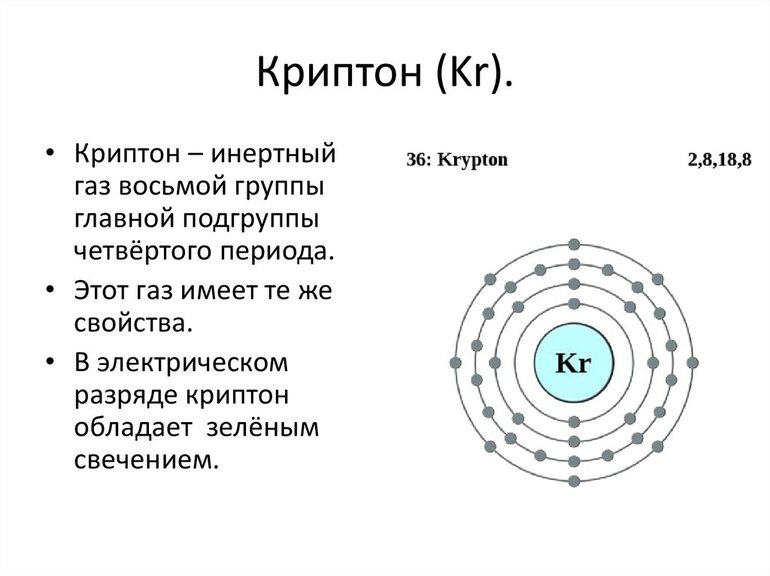
К категории благородных газов относятся такие элементы таблицы Менделеева, как гелий, неон, аргон, криптон, ксенон и радиоактивный радон. Все эти вещества с большим трудом вступают в химические реакции, за что они и получили свое второе название – инертные. Объясняется это обстоятельство тем, что внешние атомные оболочки каждого из названных газов (кроме гелия) «укомплектованы» восемью электронами, создающими своего рода энергетическую стабильность.
В природе выше всего содержание благородных газов в воздухе, но они присутствуют в небольшом количестве также в горных породах ископаемых, воде, природных летучих соединениях и нефти. Встречаются они также и за пределами нашей планеты. Так, гелия, например, очень много в космическом пространстве, Солнце и вовсе состоит из него почти на 10%. Названные вещества, согласно исследовательским данным, содержатся также в атмосферах крупных планет нашей Солнечной системы.
Инертные газы, за исключением гелия и радона, добываются путем сжижения воздуха и его последующего фракционного разделения. Гелий же является сопутствующим продуктом, получаемым при добыче природного газа. Чтобы получить радон, специалисты используют соли радия-226, через которые продувается воздух. Полученное летучее соединение впоследствии тщательно фильтруется, очищается от химически активных веществ и конденсируется жидким азотом.
Инертные газы не обладают каким-либо цветом, вкусом или запахом, их невозможно почувствовать, а потому радон, например, являющийся радиоактивным веществом, представляет особую опасность. В некотором количестве благородные газы всегда присутствуют в атмосфере, но весьма плохо растворяются в воде. Они не горят и не могут поддержать горения.
Эти элементы периодической таблицы Менделеева очень хорошо проводят ток и при этом светятся, но обладают высокими теплоизоляционными свойствами. В реакции с металлами, кислородом, щелочами, кислотами и различными веществами вступают плохо, однако чем больше их атомная масса, тем интенсивнее и химическая активность.
Такие благородные газы, как гелий и неон вступают в реакции с другими веществами исключительно при искусственно созданных и очень сложных для воплощения условиях. Куда охотнее реагируют на другие соединения ксенон, криптон и радон, поэтому к настоящему времени химикам удалось получить множество соединений с их участием.
Инертные газы не являются ядовитыми, однако все они обладают способностью вытеснять кислород из воздушных масс, а потому могут понизить его концентрацию в помещении до смертельно низкого для человека уровня. Кроме того, смеси, в состав которых входят тяжелые благородные газы и кислород, воздействуют на человека подобно наркотикам, а потому при работе с ними строго обязательно использовать все необходимые средства защиты и постоянно отслеживать состав воздуха в помещении.
Радон же, как мы уже упоминали, является радиоактивным газом, который образуется в процессе природного распада урана; обнаруживается во всех разновидностях горных пород, а также почве. Присутствовать радон может и в воде. Тем не менее после попадания газа в атмосферу его концентрация быстро падает до очень низкого уровня, поэтому, как правило, он не представляет опасности.
Благородные газы весьма широко применяются в таких отраслях человеческой деятельности, как металлургия, строительство, авто – и машиностроение, коммунальной сфере и т. д. Нерадиоактивные инертные газы также используются для наполнения цветных газозарядных трубок, с помощью которых производятся уличные вывески, реклама, лампы для загара, а также лампы дневного света.
Жидкий гелий применяется для научных исследований, которые могут производиться лишь при сверхнизких температурах, так как он является самой холодной жидкостью на планете. С его помощью в электромагнитах создается эффект сверхпроводимости, необходимый для аппаратов магнитно-резонансной томографии, ядерных ускорителей и т. д. В газообразном же состоянии это вещество, не вызывающее наркотических отравлений, применяется также при создании дыхательных смесей для аквалангов, заполнении дирижаблей, зондов и воздушных шаров. В некоторых случаях смеси гелия и кислорода могут применяться в медицине для терапии болезней дыхательной системы.
Неон используется для создания радиоламп, а в смеси с гелием преобразуется в рабочую среду газовых лазеров. В жидком состоянии его используют для охлаждения различных субстанций. Аргон – газ, имеющий широкую область применения из-за своей низкой цены. Его используют при создании инертной атмосферы, необходимой для проведения соответствующих манипуляций с цветными и щелочными металлами, кроме того, им наполняют люминесцентные и электрические лампы.
Криптон, как и аргон, обладает крайне низкой теплопроводностью, поэтому используется для заполнения стеклопакетов, а также специальных ламп, использующихся в лазерах. Ксеноном также наполняют лампы, но уже для проекторов и прожекторов. Этот же газ успешно эксплуатируют в ходе рентгеноскопии головного мозга и кишечника.
Благородные газы – полезные и очень древние вещества, существовавшие во вселенной еще до появления нашей планеты. Как мы упоминали, из одного из них, гелия, на 10% состоит звезда, дающая Земле жизнь – Солнце. Много гелия содержится также в атмосфере Юпитера – планеты, считающейся самой большой в нашей солнечной системе, однако далеко не самой крупноразмерной в известной человечеству вселенной. О каких еще колоссах космоса знают ученые и каковы их реальные размеры, мы рассказали тут.
Благородные (инертные) газы.
Благородные газы (инертные либо редкие газы) — группа химических элементов с похожими свойствами: при нормальных условиях они являются одноатомными газами. Это химические элементы, которые образуют главную подгруппу 8-й группы периодической системы Менделеева.
Среди всех благородных газов лишь у Rn нет стабильных изотопов и только он является радиоактивным химическим элементом.
Редкими (инертными) газами являются:
В последнее время к этой группе также причисляют унуноктий (Uuo) (118).
Все инертные газы собой завершают соответствующий период в Периодической системе и имеют полностью завершенный, устойчивый внешний электронный уровень.
У инертных газов электронная конфигурация ns 2 np 6 (у гелия 1s 2 ) и они образуют VIIIА группу. С возрастанием порядкового номера увеличиваются радиусы атомов и их способность к поляризуемости, что приводит к увеличению межмолекулярных взаимодействий, к увеличению Тпл и Ткип, к улучшению растворимости газов в воде и других растворителях. Для инертных газов существуют такие известные группы соединений: молекулярные ионы, соединения включения, валентные соединения.
Цвета и спектры инертных газов.
Цвета и спектры благородных газов. В первой строке таблицы изображены благородные газы в колбах, через которые пропущен ток, во второй — сам газ в трубке, в третьей — в трубках, которые изображают обозначение элемента в периодической таблице Менделеева.
Гелий
Неон
Аргон
Криптон
Ксенон
Распространенность инертных (редких) газов в природе.
Из-за того, что инертные газы обладают химической инертностью, их довольно долго не получалось обнаружить, и их открытие состоялось лишь во 2-й половине XIX века.
Гелий – является вторым (после водорода) по распространенности элементом во Вселенной, в земной коре содержание гелия составляет лишь 1 · 10-6 масс. %. Гелий является продуктом радиоактивного распада и содержится в пустотах горных пород и в природном газе.
Все благородные газы являются составляющими воздуха. В 1 м 3 воздуха находится 9,3 л аргона, 18 мл неона, 5 мл гелия, 1 мл криптона и 0,09 мл ксенона. Солнце приблизительно на 10% состоит из гелия, образующийся из водорода по реакции ядерного синтеза:
В небольшом количестве они присутствуют в воздухе и некоторых горных породах, а также в атмосферах некоторых планет-гигантов.
Промышленное использование инертных газов основано на их низкой химической активности или специфических физические свойствах.
Некоторые характеристики элементов VIIIА подгруппы (инертных газов).
Элемент
Радиус атома, нм
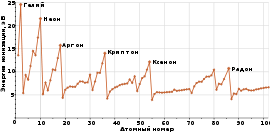
Первый потенциал ионизации, эВ
Tпл., K
Tкип., K
Относительная поляризуемость атома, усл. ед.
Энергия возбужденного электрона, эВ
Инертные газы
Содержание
Химические свойства
Физические свойства
Инертные газы бесцветны и не имеют запаха. В небольшом количестве они присутствуют в воздухе и некоторых горных породах, а также в атмосферах некоторых планет-гигантов.
Биологическое действие
Вдыхание радиоактивного радона может вызвать рак.
Применение
Инертные газы имеют очень низкие точки кипения и плавления, что позволяет их использовать в качестве холодильного агента в криогенной технике. В частности, жидкий гелий, который кипит при 4,2 К (−268,95 °C; −452,11 °F), используется для магнитной сверхпроводимости, которая используется для магнитно-резонансной томографии и ядерного магнитного резонанса. Жидкий неон хотя и не достигает таких низких температур как жидкий гелий, также находит применение в криогенике, потому что у него охлаждающие свойства более чем в 40 раз выше, чем у жидкого гелия и более чем в три раза выше, чем у жидкого водорода.
Гелий используется как компонент дыхательного газа (дыхательной смеси) вместо азота, благодаря пониженной растворимости в жидкостях, особенно в липидах. Газы поглощаются кровью и биологическими тканями, когда они находятся под давлением, как например в подводном плавании, что является причиной эффекта, известного как азотное отравление. Благодаря меньшей растворимости, маленький гелий задерживается клеточной мембраной, и поэтому гелий используется в дыхательных смесях, таких как тримикс и гелиокс, уменьшая наркотический эффект газов, возникающий на глубине. Пониженная растворимость гелия даёт другие выгоды в условии, известном как декомпрессионная болезнь. Уменьшение остатка растворённого газа в теле означает, что меньшее количество газовых пузырьков образуется во время всплытия. Другой инертный газ, аргон, рассматривается как лучший выбор для использования в качестве прослойки к сухому костюму [6] для подводного плавания, а также в больших количествах используется для обработки жидкой стали.
После крушения дирижабля Гинденбург в 1937, гелий заменил водород в качестве поднимающего газа в дирижаблях и воздушных шарах благодаря лёгкости и невоспламеняемости, несмотря на 8,6 % уменьшение плавучести (buoyancy).
Открытие и список инертных газов
Инертные газы относятся к 18-й группе химических элементов периодической таблицы Менделеева. Всего существует 6 элементов, которые имеют следующие названия и формулы:
Они довольно широко представлены во вселенной. По современным подсчетам космическая масса вселенной состоит на 76% из водорода, на 23% из гелия и только 1% приходится на другие элементы.
Водород и гелий ученые относят к элементам первичной материи вселенной. В атмосфере Земли благородных газов около одного процента. В основном это аргон. Их открытие — одна из увлекательнейших страниц истории науки.
Содержание инертных газов в природе:
Первым из этих элементов был открыт гелий. В 1868 году его обнаружили в солнечном спектре. В Парижской академии газ назвали гелий или «солнечный». Британский химик Уильям Рамзай открыл гелий и на Земле, но уже после того, как был открыт аргон.
В 1892 году в Лондоне химик Джон Уильям Стретт (лорд Рэлей) опубликовывает обращение к ученым в журнале «Природа». Он обнаружил, что азот, полученный из воздуха, имеет больший вес, чем азот, полученный химическим путем. Как объяснить это явление — задал Рэлей вопрос своим коллегам?
Рамзай высказал предположение: в азоте воздуха содержится неизвестный газ. Два года совместных исследований привели к сенсационным результатам. Был открыт новый газ, он оказался инертным. Он стал называться аргон — «медленный» или «неактивный».
Физические свойства
Менделеев открытие аргона расценивал как испытание периодического закона. Ведь если аргон существует, то он должен стоять на месте калия, однако это противоречило бы закону периодической повторяемости свойств элементов.
Испытание было выдержано с успехом. Открытие гелия на Земле позволило предположить наличие отдельной группы. Из-за инертности газов их выделили в нулевую группу. Рамзай был непоколебимым сторонником периодического закона Менделеева и, опираясь на него, предсказал, а потом уже открыл неон, криптон и ксенон.
Радон был обнаружен в 1900 году, как результат распада радиоактивного радия. Сам он также подвергался дальнейшему распаду. Превращаемость элементов, стала доказанным фактом и новые открытия, обусловленные развитием техники.
Инертные газы имеют следующие физические свойства:
При помощи масс-спектрографа у всех инертных газов обнаружены изотопы. В природе у гелия наименьшее количество стабильных изотопов — 2, у ксенона — наибольшее 9. У радона стабильных изотопов не обнаружено.
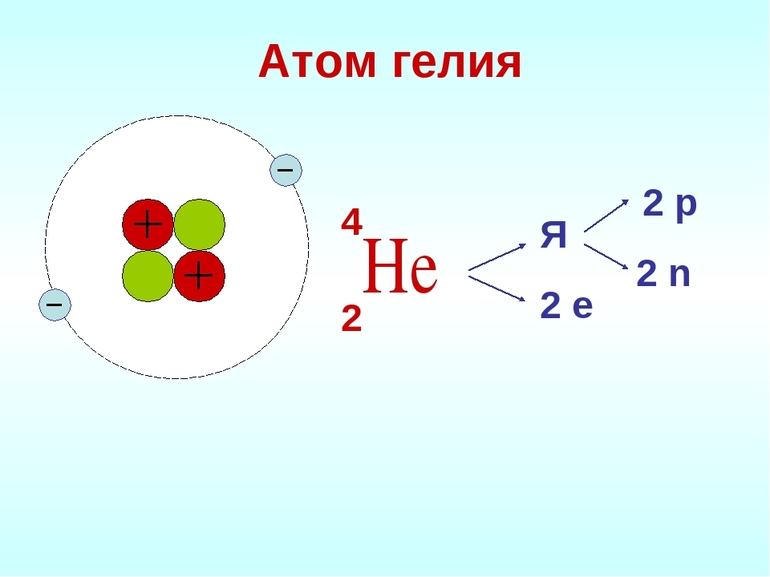
Строение атомов
Причина инертности благородных газов в строении атомов. Исследования показали, что у них максимально заполненные энергетические уровни. Гелий обозначается как 1s 2 элемент. Он имеет самую прочную структуру атома среди всех химических элементов.
Остальные благородные газы — это p элементы. Электронное строение атома определяет многие свойства этих газов. Их молекулы одноатомные. У них низкая энергия сродства к электрону.
Завершенность внешнего энергетического уровня обусловливает диамагнитность благородных газов. Высокие потенциалы ионизации, также прямое следствие замкнутости и устойчивости электронных оболочек атомов.
С ростом порядкового номера элемента его потенциал ионизации уменьшается. При сравнении видно, что начиная с криптона, у инертных газов ионизационный потенциал уже ниже, чем у кислорода и фтора. Это обусловливает возможность взаимодействия этих элементов.
Опровержение теории химической инертности
По плотности они делятся на легкие: гелий и неон и тяжелые — все остальные. Гелий самый легкий газ в природе, он легче воздуха в 7 раз. Аргон открывает группу тяжелых газов. Жидкий аргон тяжелее не только воздуха, но и воды.
С увеличением поляризуемости от гелия к радону, увеличиваются радиусы атомов, а также возрастает растворимость в воде и абсорбируемость. Газообразный гелий с трудом можно собрать в закрытый сосуд. Аргон, по сравнению с гелием, уже более вязкий. Его можно перелить из сосуда в сосуд. С увеличением атомной массы и радиуса атома у газов уменьшается теплопроводность, повышается температура кипения. Кроме того, увеличивается возможность деформации внешних электронных слоёв, а значит создается предпосылка химической связи.
Для сжижения благородных газов нужны сверхнизкие температуры, особенно для гелия. У жидкого гелия обнаружено уникальное свойство — сверхтекучесть.
Это подтверждается простым опытом. Если погрузить пробирку в сосуд с жидким гелием, то жидкость будет ползти вверх по наружной стенке пробирки и опускаться по внутренней. Если пробирку приподнять, то гелий начинает двигаться в обратную сторону, выравнивая уровни. Когда пробирку вынимают, то гелий продолжает стекать по ней и капать вниз.
Это свойство у гелия открыл советский физик, академик Петр Леонидович Капица. В 1962 году канадский химик Нил Бартлетт, наконец, опроверг теорию химической инертности благородных газов. Ему удалось в процессе гетерогенного катализа синтезировать соединение ксенона с гексафторидом платины (Xe+PtF6=Xe (PtF6)x).
Событие это было также сенсационно, как заявление Рамзая об инертности аргона. Это позволило инертным газам покинуть нулевую группу. Инертные газы в таблице Менделеева справедливо заняли свое место в восьмой группе.
Правда, еще до открытия Бартлетта были получены клатратные соединения тяжелых инертных газов. При относительно высоких давлениях молекулы газов, в этом случае криптона, плотно окружаются молекулами гидрохинона и включаются в них.
В клатратных соединениях связь молекулярная, валентные электроны в них не взаимодействуют. Клатраты нестойкие соединения, в растворах они быстро распадаются на составные части. Их можно использовать как удобные формы для хранения благородных газов.
Фториды и оксиды ксенона
После работ Бартлетта, следующим шагом стали явились опыты по непосредственному соединению ксенона с фтором. Из смеси одного объема ксенона, варьируя условия реакции, получают фториды с различной степенью окисления ксенона. Самый устойчивый из них — тетрафторид ксенона.
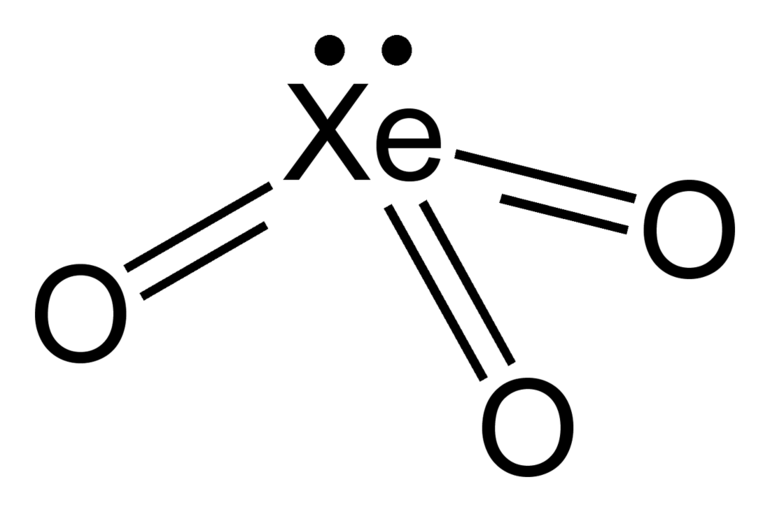
Фториды ксенона довольно летучие вещества. Хранят их в тефлоновых сосудах. Они хорошие окислители и фторирующие агенты. Фториды ксенона подвержены гидролизу. В результате реакции образуются оксофториды или оксиды. Триоксид ксенона в сухом виде легко взрывается. Сила взрыва такая же, как у тротила.
Оксиды обладают кислотными свойствами. При взаимодействии с основаниями образуют соли. Триоксид образует ксенаты. Реакция диспропорционирования ксенатов приводит к образованию перксенатов. Ксенаты являются солями ксенонистой кислоты, а перксенаты — ксеноновой. Ксеноновая кислота, в свою очередь, является производной тетраоксида ксенона.
Оксиды ксенона, так же как и фториды, являются сильными окислителями. При реакции с йодом калия образуется йод и ксенон. Кристаллы дифторида ксенона можно получить, если смесь газов в кварцевой ампуле подвергнуть ультрафиолетовому облучению. Его можно получить также при помощи электрического разряда.
Химия инертных газов — это прежде всего химия ксенона. Это синтезированные и комплексные соединения фторидов, полученные катионные и анионные формы комплексов.
Получение и использование аргона
В промышленности благородные газы получили широкое применение. Наиболее доступный из них — аргон. Его получают из воздуха методом двойной ректификации при низких температурах. Воздух очищают от углекислоты и влаги, сжижают с помощью глубокого холода и подают в ректификационную колонну.
Сравнительно легко выделяют азот, а вот с кислородом труднее. Температура кипения его и аргона близки. Способом двойной ректификации кислород отделяется, и сырой аргон поступает в блок тонкой адсорбционной очистки.
Адсорбция идет на синтетических цеолитах, так называемых молекулярных ситах. Благодаря этому методу аргон получается очень чистым, практически без примеси.
Основная область применения аргона — металлургическая и металлообрабатывающая промышленность. Аргонодуговая сварка очень высокопроизводительна и обеспечивает хорошее качество шва.
Другой способ получения аргона, а также криптона и ксенона основан на методе адсорбции из отходящих газов при синтезе аммиака.
Использование в промышленности гелия и радона
Гелий получают из природных газов, которые предварительно очищаются от примесей и влаги.
Сухой газ, проходя несколько этапов, охлаждается до такой температуры, когда все его компоненты конденсируются в жидкость, лишь гелий остается газообразным. Через верхнюю часть разделительного аппарата он выводится наружу. Налажено производство и жидкого гелия. Он играет большую роль в современной физике и криогенной технике.
В газообразном виде легкий и инертный гелий — идеальный наполнитель для дирижаблей. Благодаря налаженному промышленному получению гелия, идея дирижаблестроения в стране возрождается.
Находят применение и радиоактивные изотопы благородных газов. Радиоизотопы ксенон-133 используется для исследования спинного мозга и кровотока головного мозга. Прибор, регистрирующий радиоактивность, определяет локализацию изотопа ксенона и помогает ставить правильный диагноз.
Радон — радиоактивный газ, он дочерний элемент изотопа радия-226. Используя хорошую растворимость радона в воде, медицина поставила его на службу человека. Растворенный радон диффундирует через кожу и оказывает благотворительное воздействие на центральную нервную систему, а через нее и на другие органы человека. Поэтому широко распространено лечение радоновыми ваннами.
В геологии изотопом аргон-40 определяют абсолютный возраст горных пород по методу советского ученого Герлинга. В основе метода лежит процесс распада радиоактивного изотопа калия-40 с образованием основного изотопа аргона-40.
В электровакуумной промышленности используют свойство инертных газов светиться, если через них пропускать электрический разряд. Промышленность выпускает очень широкий ассортимент газоразрядных источников света.
На основе изучения благородных газов складывался ряд фундаментальных научных законов. Все отчетливее выявляется их значение в познании Земли и космоса.